
【题目】80年代,科学研制得一种新分子,它具有空心的类似足球状的结构,分子式为C60 . 下列说法正确的是( )
A.C60是一种新型的化合物
B.C60含有离子键
C.C60和金刚石互为同位素
D.C60中的化学键只有共价键
科目:高中化学 来源: 题型:
【题目】某同学设计用下图的装置制备少量的AlCl3(易水解)。下列说法错误的是( )
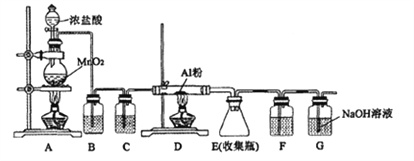
A. B装置中所装试剂为饱和的NaCl溶液,其作用是除去氯气中的HCl
B. 装置C和F中的试剂均为浓硫酸,其作用是防止水蒸气进人E中
C. 用50mL12mol/L的盐酸与足量的MnO2反应,所得氯气可以制取26.7gAlCl3
D. 实验过程中应先点燃A处的酒精灯,待装置中充满黄绿色气体时再点燃D处的酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知MnO2为黑色难溶于水的固体,实验室制取氧气的反应为2KClO3![]() 2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )
2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )
A. 溶解、过滤、蒸发、洗涤 B. 溶解、过滤、洗涤、加热
C. 溶解、蒸发、洗涤、过滤 D. 溶解、洗涤、过滤、加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的电离方程式书写正确的是
A. Na2CO3 = Na2+ + CO32
B. NaHCO3 = Na+ + H+ + CO32
C. H2CO3 = 2H+ + CO32
D. Ba(OH)2 = Ba2+ + 2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种易溶于水的白色固体,分别由Na+、Ba2+、Cu2+、Ag+、Cl-、SO42-、CO32-、NO3-中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A__________;D__________。
(2)写出下列反应的离子方程式:
①B+D→:________________;③C+HCl→气体:_______________。
(3)在作实验反思时,有同学提出:如果溶液中同时存在CO32- 和Cl-,CO32- 会对Cl- 的检验产生干扰。为了确定该溶液中是否存在Cl-,该小组同学进行了如下探究实验:
 _________________________________
_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦ 蔗糖 其中属于电解质的是(填序号)___________,
(2)写出Al2(SO4)3的电离方程式:___________________,
(3)写出NaHSO3(aq) 与稀盐酸反应的离子方程式:_____________________,
(4)胶体是一种常见的分散系,回答下列问题:
①向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为__________________。
②向Fe(OH)3胶体中加入K2SO4饱和溶液,由于SO42-的作用,使胶体形成了沉淀,这个过程叫做胶体的_______。
③区分胶体和溶液常用的方法叫做__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为实验室某浓盐酸试剂瓶上标签的有关内容。取该盐酸10mL,加蒸馏水稀释至250mL,向其中加入mg锌粉恰好完全反应。
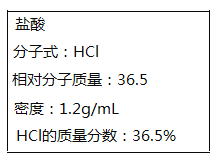
(1)写出锌粉与盐酸反应的离子方程式______________。
(2)求原浓盐酸的物质的量浓度c=____________。
(3)计算出m=___________。
(4)反应中生成的H2可以和标准状况下______mL的O2恰好完全反应。
(5)向反应后的溶液中加入0.6mol/L的AgNO3溶液至不再产生沉淀,共消耗VmL AgNO3溶液,则V的值是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 同分异构体之间分子式相同,其式量也一定相等;式量相等的物质一定是同分异构体
B. 某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃
C. 分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以初步推测有机物结构简式为CH3CH2OH
D. 分子式为C8H10的芳香烃有4种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
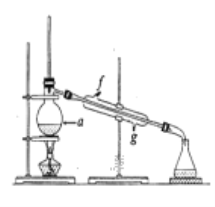
【题目】某化学小组采用下图所示的装置,用环己醇制备环己烯。
已知: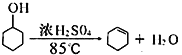
相对分子质量 | 密度/g cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 82 | 0.81 | -103 | 83 | 难溶于水 |
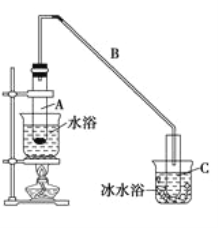
(1)制备粗品
将12.5 mL环己醇与1mL浓硫酸加入试管A中,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①在试管中混合环已醇和浓硫酸操作时,加入药品的先后顺序为______________________。
②如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是_________(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
③将试管C置于冰水中的目的是_______________________________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。向粗品中加入饱和食盐水,振荡、静置、分层,环己烯在_______层(填“上”或“下”),分液后用________(填字母)洗涤。
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将提纯后的环己烯按如图所示装置进行蒸馏。图中仪器a 的名称是_______________,实验中冷却水从______(填字母)口进入。蒸馏时要加入生石灰,目的是__________________________。
(3)若在制备粗品时环已醇随产品一起蒸出,则实验制得的环己烯精品质量_______(填“高于”、“ 低于”)理论产量。本实验所得到的环已烯质量为6.5g,则产率是______(保留一位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com