
| A、1.5 mol?L-1 |
| B、1 mol?L-1 |
| C、0.5 mol?L-1 |
| D、0.25 mol?L-1 |
| V |
| Vm |
| n |
| V |
| 1.12L |
| 22.4L/mol |
| 0.1mol |
| 0.1L |


科目:高中化学 来源: 题型:
| A、常温时的水溶性:Na2CO3<NaHCO3 |
| B、等物质的量时与足量酸反应产生CO2的量:Na2CO3>NaHCO3 |
| C、与等浓度稀盐酸反应的快慢:Na2CO3<NaHCO3 |
| D、同质量时消耗盐酸的量:Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、BeCl2溶液 pH>7,将其蒸干,灼烧后可得到BeCl2晶体 |
| B、BeCl2溶液能导电,说明BeCl2一定是离子化合物 |
| C、Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
| D、Be只能与盐酸反应,不能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在上述反应中,电子从氧化剂转移到还原剂 |
| B、物质甲可能是KMnO4 |
| C、反应中若产生3.0g气体,则转移电子数约为0.3×6.02×1023 |
| D、氧化过程的反应式一定为Cu2O-2e-+2H+═2Cu2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.4 | B、4.8 |
| C、3.2 | D、2.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、易溶于水 | B、难溶于水 |
| C、属于硅酸盐 | D、属于复盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
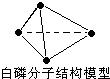
| A、31g 白磷分子(P4)中含有P-P键个数为1.5×6.02×1023 |
| B、48gO2和48gO3所含分子数为3×6.02×1023 |
| C、1.0L 1mol/L氨水中,NH3?H2O的分子数为6.02×1023 |
| D、20g 重水(D2O)中含有的中子数为8×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.l mol?L-1的NaAlO2溶液:K+、Na+、SO42-、CO32- |
| B、使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl- |
| C、含有大量ClO-溶液中:K+、OH-、I-、SO32- |
| D、c(Al3+)=0.1 mol?L-1的溶液中:Na+、Cl-、AlO2-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com