
【题目】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达式均正确的是( )

A.①是其他条件一定时,反应速率随温度变化的图象,正反应△H<0
B.②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图象
C.③是在有无催化剂存在下建立的平衡过程图象,a是使用催化剂时的曲线
D.④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1>p2
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】已知阿伏伽德罗常数可表示为NA,则下列说法正确的是
A. 任何气体单质在标准状况下体积约为22.4L,则一定含有2NA个原子
B. 常温常压下,22g氧气和26g臭氧所含氧原子总数为3NA
C. 常温常压下,22.4LH2O中含有的氢原子数为2NA
D. 标准状况下,0.3molCO2中含有氧原子数0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体内有20多种微量元素,它们的质量总和不到体重的千万分之一,但是对人的健康却起着重要的作用,下列各组元素全部是微量元素的是( )
A. Na K Cl S O
B. F I Fe Zn Cu
C. N H O P C
D. Ge Ca Cu Mg C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】


(1)写出下列仪器的名称:① ② .
(2)仪器①~④中,使用时必须检查是否漏水的有 .(填序号)
(3)若利用装置I分离丙三醇(能跟水、酒精以任意比互溶,沸点290℃)和酒精(沸点78.2℃)的混合物,还缺少的仪器有 ,将仪器补充完整后进行的实验操作的名称为; .进水方向是 (填g或f),还需加入少量碎瓷片,其作用是 .
(4)如图所示装置Ⅱ是转移操作,请指出该操作错误之处: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有广阔的海岸线,建设海峡经济区,海水的综合利用大有可为,下图所示为海水综合利用部分流程,有关说法正确的是( )
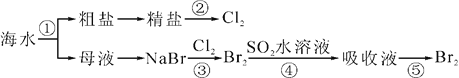
A. 上述工艺流程中涉及到化合、分解、复分解和置换反应
B. ①只发生了化学变化,②是工业上用电解熔融NaCl制备Cl2
C. ③④涉及的反应均为氧化还原反应,⑤只需要蒸馏即可得到单质Br2
D. ④中反应的离子方程式为SO2+Br2+2H2O===4H++SO42-+2Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量分数为36.5%的盐酸(密度为1.16gcm﹣3)配制1molL﹣1的稀盐酸.现实验室仅需要这种盐酸220mL,试回答下列问题:
(1)配制稀盐酸时,除了用到量筒、烧杯、玻璃棒、胶头滴管,还需使用的玻璃仪器有 。
(2)计算已知盐酸的物质的量浓度为 。
(3)经计算需要 mL浓盐酸,在量取时宜选用下列量筒中的 。
A.5mL | B.10mL | C.25mL | D.50mL |
(4)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入250mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号) 。
(5)在上述配制过程中,若定容时水加多后用滴管吸出多余的部分,则配制的稀盐酸浓度是 (填“偏高”、“偏低”或“无影响”);若定容时俯视刻度线,则配制的稀盐酸浓度是 (填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)已知下列反应:SO2 (g)+2OH–(aq) =SO32–(aq)+H2O(l) ΔH1;
ClO–(aq)+SO32–(aq)=SO42–(aq)+Cl–(aq) ΔH2;
CaSO4(s)=Ca2+(aq)+SO42–(aq) ΔH3。
则反应SO2(g)+Ca2+(aq)+ClO–(aq)+2OH–(aq)=CaSO4(s)+H2O(l)+Cl–(aq)的ΔH=______________。(用ΔH1、ΔH2、ΔH3表示)
(2)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,用甲烷制备合成气的反应为:①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-72 kJ·mol﹣1;
②CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH2=+216 kJ·mol﹣1。现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
若x=0.2时,反应①放出的能量为________kJ;
若x=_________时,反应①与②放出(或吸收)的总能量为0。
(3)一定条件,在水溶液中1 mol Cl-和1 mol ClOx(x=1,2,3,4)的能量(kJ)相对大小如图所示。

①D是________(填离子符号)。
②B→A+C反应的热化学方程式为_______________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等量的氢氧化钠溶液分别用pH=2和pH=3的醋酸溶液中和,设消耗醋酸溶液的体积依次为Va 、Vb,则两者的关系正确的为
A.Va > 10 Vb B.Vb = 10Va C.Vb < 10 Va D.Vb > 10 Va
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com