
| A�� | �٢ڢۢ� | B�� | �٢ڢ� | C�� | �ڢۢ� | D�� | �٢ۢ� |
���� ������ؾ���ǿ�����ԣ���ɱ��������������ر���ԭ����Fe3+��ˮ�����ɾ��������Ե�Fe��OH��3������ﵽ��ˮ���ã�
��� �⣺������ؾ���ǿ�����ԣ���ɱ������������������ԭ��Ӧ��������ر���ԭ����Fe3+��ˮ�����ɾ��������Ե�Fe��OH��3������ﵽ��ˮ���ã��漰����۳�������ˮ�⣬���漰��ɫ��Ӧ����۴���
�����漰���Т٢ڢܣ�
��ѡB��
���� ���⿼�������ص������Լ���Ӧԭ������Ŀ�ѶȲ�������Ĺؼ��ǰ���������ʵ����ʼ�Ӧ�ã�ѧϰ��ע����ۣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ӵ����ģ��  | B�� | ȩ���ĵ���ʽ  | ||
| C�� | ����Ľṹ��ʽ C2H4O2 | D�� | ��ϩ�����ʽΪ CH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ����ȩ������1��̼ԭ�ӡ�2����ԭ�ӡ�1����ԭ�ӹ��ɵ� | |
| B�� | ��ȩ��̼���⡢������Ԫ�ص�������Ϊ1��2��1 | |
| C�� | ��ȩ��̼���⡢������Ԫ����ɵ� | |
| D�� | ��ȩ����Ԫ�ص���������Ϊ53.3% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ����� | a | b | c |
| ��Ʒ������g�� | 9.6 | 12.8 | 64.0 |
| ���������L�� | 5.04 | 6.72 | V |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ʵ������ | ���� |
| A | SO2ͨ�����Ը��������Һ | ���Ը��������Һ��ɫ | SO2���л�ԭ�� |
| B | ��NaSiO3��Һ���Թ��еμ�1�η�̪��Ȼ����μ���ϡ��������ɫ��ȥ | 2min���Թ���������� | �ǽ����ԣ�Cl��Si |
| C | ��ʢ��ͭƬ�������м���Ũ���� | ������������ɫ���壻��Һ��Ϊ����ɫ | Ũ�������ǿ������ |
| D | Ũ����ε�ʪ��������� | ���DZ�ɺ�ɫ����״ | Ũ���������ˮ�Ժ�ǿ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ20����ԭ�ӣ�${\;}_{17}^{37}$Cl | |
| B�� | ̼����ˮ������ӷ���ʽ��CO32-+2H2O?OH-+H2CO3 | |
| C�� | CH3COOH�ĵ��뷽��ʽΪ��CH3COOH+H2O?CH3COO-+H3O+ | |
| D�� | ������Ľṹʽ��H-O-Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����������� | ���� |
| A | ȡ������������Һ�������м�������������ˮ���ڵμ�KSCN��Һ����Һ��Ѫ��ɫ | ����Һ�к���Fe3+ |
| B | �����£���Ũ�Ⱦ�Ϊ0.1mol•L-1��BaCl2��CaCl2�����Һ�еμ�Na2SO4��Һ�����ְ�ɫ������ | Ksp��Ba2SO4����Ksp��Ca2SO4�� |
| C | �����£���FeCl3��Һ�еμ�����KI��Һ���ٵμӼ��ε�����Һ����Һ����ɫ | Fe3+�������Ա�I2��ǿ |
| D | �����£���PH��ֽ��ã�0.1mol•L-1 Na2SO3��Һ��PHԼΪ10��0.1mol•L-1 NaHSO3��Һ��PHԼΪ5 | HSO3-���H+��������SO32-��ǿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�м����������������ú��ϲ���ɫ��dz���²���ɫ��Ϊ�Ϻ�ɫ | |
| B�� | ���ȵ�ͭ˿��������ȼ�գ��������ػ�ɫ������ | |
| C�� | ±�ص��ʣ�X2����ˮ��Ӧ������X2+H2O=HX+HXO��ʾ | |
| D�� | �廯����Һ�м����������Ƶ���ˮ���ټ����������Ȼ�̼�����ú��ϲ���ɫ��dz���²���ɫ��Ϊ�Ⱥ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
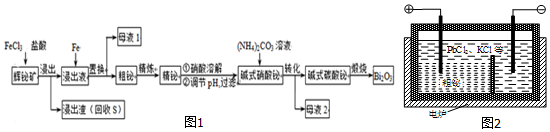
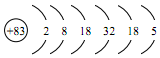 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com