
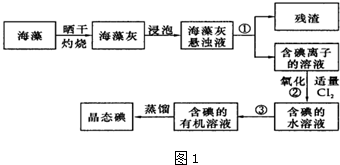
分析 海带晒干灼烧可生成水和二氧化碳,海带灰中含有碘化钾等物质,溶于水,浸泡过滤得到含有碘离子的溶液,加入氯水或通入氯气,氯气置换出碘,得到碘的水溶液,用四氯化碳或苯萃取得到含碘的有机溶液,经蒸馏可得到碘,以此解答该题.
(1)固体和液体分离用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来用萃取,萃取后分液;氯气可以将碘离子氧化为单质碘;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,据此来选择合适的试剂;
(3)碘在四氯化碳中的溶解度大于在水中的溶解度,能将碘水中的碘转移到四氯化碳中,四氯化碳的密度比水大,溶解碘后溶液为紫红色;
(4)据蒸馏装置图分析判断,根据实验原理选择合适的仪器;
(5)大面积玻璃容器加热需要垫石棉网,温度计水银球应与烧瓶支管口相平;冷凝水应是下进上出;
解答 解:(1)操作①海带灰悬浊液通过过滤得到含碘离子的溶液,操作③碘在水中的溶解度小于在有机物中的溶解度,可用萃取然后分液得到含碘的有机溶液;氯气可以将碘离子氧化为单质碘,离子方程式为:Cl2+2I-═2Cl-+I2;
故答案为:过滤;萃取分液;Cl2+2I-═2Cl-+I2;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,故可用四氯化碳、苯或直馏汽油,酒精、乙酸等和水是互溶的,不能选择,
故答案为:B;
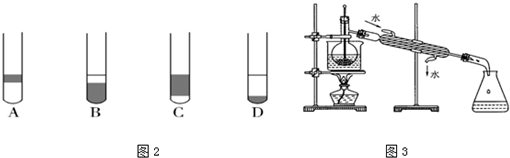
(3)碘在四氯化碳中的溶解度大于在水中的溶解度,能将碘水中的碘转移到四氯化碳中,四氯化碳的密度比水大,溶解碘后溶液为紫红色,所以在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是溶液分层,上层颜色接近无色,下层呈紫红色;
故选D,
故答案为:D;
(4)为使海藻灰中碘离子转化为碘的有机溶液,应使用过滤、萃取分液和蒸馏等操作完成,根据实验装置原理,使用的仪器有:烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、漏斗,分液漏斗等,
故答案为:普通漏斗 分液漏斗.
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,存在的错误有:①温度计水银球应与烧瓶支管口相平;②冷凝水应是下进上出;③装置中烧杯底部未垫石棉网,水浴加热的烧杯下需要垫石棉网,加热均匀,
故答案为:温度计下端的水银球不能插入溶液中,应放在支管口;冷凝管中水流方向相反了;没有石棉网;
点评 本题考查物质的分离和提纯,题目难度中等,学习中注意蒸馏、萃取的原理,掌握基础是解题关键.


科目:高中化学 来源: 题型:推断题
 有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系:
有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、Al3+、S2-、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | K+、SO42-、HCO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、R、D都是周期表中前四周期的元素,它们的原子序数依次增大.其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素.
已知A、B、R、D都是周期表中前四周期的元素,它们的原子序数依次增大.其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
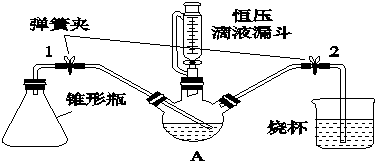
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
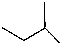 ,下列有关叙述正确的是( )
,下列有关叙述正确的是( )| A. | 该烃的分子式是C5H10 | B. | 与C4H10互为同系物 | ||
| C. | 分子中只有极性共价键 | D. | 能与溴水反应使其褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有①④⑤ | C. | 只有③④ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com