
”¾ĢāÄæ”æX”¢Y”¢W”¢Z ŹĒĖÄÖÖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ĖęŌ×ÓŠņŹż±ä»ÆČēÓŅĶ¼ĖłŹ¾”£ŅŃÖŖ W µÄŅ»ÖÖŗĖĖŲµÄÖŹĮæŹżĪŖ 18£¬ÖŠ×ÓŹżĪŖ 10£¬XŗĶNeŌ×ÓµÄŗĖĶāµē×Ó×ÜŹżĻą²ī 1£»Y µÄµ„ÖŹŹĒŅ»ÖÖ³£¼ūµÄ°ėµ¼Ģå²ÄĮĻ£» Z µÄ·Ē½šŹōŠŌŌŚĶ¬ÖÜĘŚÖ÷×åŌŖĖŲÖŠ×īĒ攣 ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A. ×īøß»ÆŗĻ¼Ū£ŗ X£¾Y£¾Z£¾W
B. ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗ Z£¾Y£¾W
C. Y µÄŃõ»ÆĪļÓė X”¢ Z µÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ¾łÄÜ·“Ó¦
D. ÓÉ X”¢ Z”¢ W ČżÖÖŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļŅ»¶Ø¼Čŗ¬ÓŠĄė×Ó¼üÓÖŗ¬¹²¼Ū¼ü
”¾“š°ø”æD
”¾½āĪö”æŹŌĢā·ÖĪö£ŗWµÄÖŹĮæŹżĪŖ18£¬ÖŠ×ÓŹżĪŖ10£¬ŌņÖŹ×ÓŹżĪŖ(18£10)=8£¬ŌņWĪŖO£¬XŗĶNeŌ×ÓµÄŗĖĶāµē×ÓŹżĻą²īĪŖ1£¬ŌņXæÉÄÜŹĒF£¬Ņ²æÉÄÜŹĒNa£¬øł¾ŻŌ×Ó°ė¾¶£¬ŌņXĪŖNa£¬Yµ„ÖŹŹĒŅ»ÖÖ°ėµ¼Ģå²ÄĮĻ£¬ŌņYĪŖSi£¬Ķ¬ÖÜĘŚÖŠ“Ó×óĻņÓŅ·Ē½šŹōŠŌŌöĒ棬¼“ZĪŖCl£¬A”¢×īøß»ÆŗĻ¼Ū·Ö±šŹĒ0”¢£«1”¢£«4”¢£«7£¬Ņņ“Ė×īøß¼Ū»ÆŗĻ¼ŪÓɓ󵽊”µÄĖ³ŠņŹĒ£ŗCl>Si>Na>O£¬¹Ź“ķĪó£»B”¢·Ē½šŹōŠŌŌ½Ē棬ĘäĒā»ÆĪļĪČ¶ØŠŌŌ½Ē棬·Ē½šŹōŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒO>Cl>Si£¬Ēā»ÆĪļĪČ¶ØŠŌ£ŗO>Cl>Si£¬¹Ź“ķĪó£»C”¢YµÄŃõ»ÆĪļŹĒSiO2£¬XµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļŹĒNaOH£¬ZµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļŹĒHClO4£¬SiO2ŹĒĖįŠŌŃõ»ÆĪļ£¬ÓėNaOH·“Ó¦£¬²»ÄÜÓėHClO4·“Ó¦£¬¹Ź“ķĪó£»D”¢NaClO”¢NaClO3µČŹōÓŚĄė×Ó»ÆŗĻĪļ£¬ŗ¬ÓŠĄė×Ó¼üŗĶ¹²¼Ū¼ü£¬¹ŹÕżČ·”£


 ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø
ÖŠæ¼½ā¶Įæ¼µć¾«Į·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2016ÄźIUPACĆüĆū117ŗÅŌŖĖŲĪŖTS£ØÖŠĪÄĆū![]() £¬tiØ¢n£©£¬TSµÄŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżŹĒ7.ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
£¬tiØ¢n£©£¬TSµÄŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżŹĒ7.ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A. TSŹĒµŚĘßÖÜĘŚµŚ¢÷A×åŌŖĖŲ B. TSµÄĶ¬Ī»ĖŲŌ×Ó¾ßÓŠĻąĶ¬µÄµē×ÓŹż
C. TSŌŚĶ¬×åŌŖĖŲÖŠ·Ē½šŹōŠŌ×īČõ D. ÖŠ×ÓŹżĪŖ176µÄTSŗĖĖŲ·ūŗÅŹĒ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒA”¢BĮ½ÖÖÓŠ»śĪļµÄÓŠ¹ŲŠÅĻ¢£ŗ
A | B |
¢Ł·Ö×ÓÄ£ŠĶĪŖ£ŗ ¢ŚÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«£» ¢ŪĘä²śĮæŹĒŗāĮæŹÆÓĶ»Æ¹¤Ė®Ę½µÄ±źÖ¾”£ | ¢ŁÓÉC”¢H”¢OČżÖÖŌŖĖŲ×é³É£¬ŹĒ³ų·æÖŠµÄ³£¼ūµ÷Ī¶¼Į£» ¢ŚĖ®ČÜŅŗÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äŗģ”£ |
øł¾Ż±ķÖŠŠÅĻ¢»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)¹ŲÓŚAµÄĻĀĮŠĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ__________(Ģī±źŗÅ)”£
a£®·Ö×ÓĄļŗ¬ÓŠĢ¼Ģ¼Ė«¼ü b£®·Ö×ÓĄļĖłÓŠµÄŌ×Ó¹²Ę½Ćę c£®½į¹¹¼ņŹ½ĪŖCH2-CH2
(2)AÓėH2·¢Éś¼Ó³É·“Ó¦ŗóÉś³ÉX£¬ÓėXŌŚ·Ö×Ó×é³ÉŗĶ½į¹¹ÉĻĻąĖʵÄÓŠ»śĪļÓŠŅ»“óĄą£¬ĖüĆĒµÄĶØŹ½ĪŖCnH2n+2”£µ±n=_________Ź±£¬ÕāĄąĆĒ»śĪļæŖŹ¼³öĻÖĶ¬·ÖŅģ¹¹ŠŻ”£
(3)BÓėŅŅ“¼·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________£¬·“Ó¦ĄąŠĶĪŖ_______________”£
(4)ŅŌAĪŖŌĮĻæÉÖ±½ÓÉś²śŅ»ÖÖøß·Ö×Ó»ÆŗĻĪļP£¬ŌņPµÄ½į¹¹¼ņŹ½ĪŖ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬Ņ»¶ØĮæµÄNa2C03ÓėŃĪĖį»ģŗĻĖłµĆČÜŅŗÖŠ£¬²æ·Öŗ¬Ģ¼Ī¢Į£µÄĪļÖŹµÄĮæ·ÖŹż(![]() )ÓėpHµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
)ÓėpHµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. ĒśĻßX±ķŹ¾µÄĪ¢Į£ĪŖCO32-
B. pH=6.3Ź±£¬![]() (CO32-)+
(CO32-)+![]() (HCO3-)+
(HCO3-)+![]() (H2CO3)=1.0
(H2CO3)=1.0
C. pH=7Ź±£¬c(HCO3-)£¾c(CO32-)£¾c(H2CO3)£¾c(OH-)=c(H+)
D. pH=10.3 Ź±£¬c(Na+)+c(H+)=c(Cl-)+c(OH-)+3c(HCO3-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠÕżČ·µÄŹĒ£Ø””””£©
A.ÓĆŹÆÄ«×÷µē¼«µē½ā±„ŗĶNaClČÜŅŗ£ŗ2Cl©+2H2O ![]() Cl2”ü+H2”ü+2OH©
Cl2”ü+H2”ü+2OH©
B.ĻņĆ÷·ÆČÜŅŗÖŠÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮAl3+øÕŗĆ³ĮµķĶźČ«£ŗ
Al3++SO42©+Ba2++3OH©ØTBaSO4”ż+Al£ØOH£©3”ż
C.¹żĮæĀČĘųĶØČėäå»ÆŃĒĢśČÜŅŗÖŠ£ŗ2Cl2+2Fe2++2Br©ØT4Cl©+2Fe3++Br2
D.ĻņĀČ»ÆĀĮČÜŅŗĶØČė¹żĮæµÄ°±Ęų£ŗAl3++4OH©ØTAlO2©+2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷ĪļÖŹ£¬°“µ„ÖŹ”¢»ÆŗĻĪļ”¢»ģŗĻĪļµÄĖ³ŠņÅÅĮŠµÄŹĒ£Ø £©
A.øɱł”¢Ģś”¢µØ·Æ
B.ŅŗĢ¬Ńõ”¢Ńõ»ÆøĘ”¢ŹÆ»ŅĖ®
C.µŖĘų”¢ĀČ»ÆĒā”¢ÉÕ¼ī
D.Ė®”¢µā¾Ę”¢ŹģŹÆ»Ņ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶس£¹¤ŅµÉĻ¼ą²āSO2ŗ¬ĮæŹĒ·ń“ļµ½Åŷűź×¼µÄ»Æѧ·“Ó¦ŌĄķŹĒ£ŗSO2 + H2O2 + BaCl2 ![]() BaSO4”ż+ 2HCl”£ÓĆNA±ķŹ¾°¢·üŁ¤µĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
BaSO4”ż+ 2HCl”£ÓĆNA±ķŹ¾°¢·üŁ¤µĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. 0.1 mol BaCl2¹ĢĢåÖŠĖłŗ¬Ąė×Ó×ÜŹżĪŖ0.3 NA
B. 25 oCŹ±£¬pH=1µÄHClČÜŅŗÖŠŗ¬ÓŠH+µÄŹżÄæŌ¼ĪŖ0.1 NA
C. ±ź×¼×“æöĻĀ£¬17 g H2O2ÖŠĖłŗ¬¹²ÓƵē×Ó¶ŌŹżĪŖ2 NA
D. Éś³É2.33 g BaSO4³ĮµķŹ±£¬ĪüŹÕSO2µÄĢå»żĪŖ0.224 L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē½āŌĄķŗĶŌµē³ŲŌĄķŹĒµē»ÆѧµÄĮ½øöÖŲŅŖÄŚČŻ”£Ä³ŠĖȤŠ”×é×öČēĻĀĢ½¾æŹµŃé£ŗ
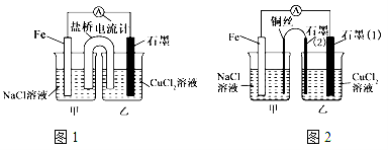
£Ø1£©ČēÉĻĶ¼1ĪŖijŹµŃ銔×éŅĄ¾ŻŃõ»Æ»¹Ō·“Ó¦Éč¼ĘµÄŌµē³Ų×°ÖĆ£¬ČōŃĪĒÅ֊װӊ±„ŗĶµÄKNO3ČÜŅŗŗĶĒķ½ŗÖĘ³ÉµÄ½ŗ¶³,ŌņNO3-ŅĘĻņ_____________×°ÖĆ£ØĢīŠ“”°¼×»ņŅŅ”±£©”£ĘäĖūĢõ¼ž²»±ä£¬Čō½«CuCl2ČÜŅŗ»»ĪŖNH4ClČÜŅŗ£¬·¢ĻÖÉś³ÉĪŽÉ«ĪŽĪ¶µÄµ„ÖŹĘųĢ壬ŌņŹÆÄ«ÉĻµē¼«·“Ó¦Ź½______________________”£
£Ø2£©ČēÉĻĶ¼2£¬ĘäĖūĢõ¼ž²»±ä£¬Čō½«ŃĪĒÅ»»³ÉĶäĶµ¼ĻßÓėŹÆÄ«ĻąĮ¬³ÉnŠĶ£¬Ōņ¼××°ÖĆŹĒ____________£ØĢī”°Ōµē³Ų»ņµē½ā³Ų”±£©£¬ŅŅ×°ÖĆÖŠŹÆÄ«£Ø2£©ĪŖ ¼«£¬ŅŅ×°ÖĆÖŠÓėĢśĻßĻąĮ¬µÄŹÆÄ«£Ø1£©µē¼«ÉĻ·¢ÉśµÄ·“Ó¦Ź½ĪŖ ”£
£Ø3£©ŌŚĶ¼2ŅŅ×°ÖĆÖŠøÄĪŖ¼ÓČėCuSO4ČÜŅŗ£¬Ņ»¶ĪŹ±¼äŗó£¬ČōijŅ»µē¼«ÖŹĮæŌöÖŲ 1.28 g£¬ŌņĮķŅ»µē¼«Éś³É______________mL£Ø±źæöĻĀ£©ĘųĢ唣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾ŹĒZnŗĶCuŠĪ³ÉµÄŌµē³Ų£¬Ä³ŹµŃéŠĖȤŠ”×é×öĶźŹµŃéŗó£¬ŌŚ¶ĮŹéæØÉĻµÄ¼ĒĀ¼æØČēĻĀ£¬ŌņæØʬÉĻµÄĆčŹöŗĻĄķµÄŹĒ

ŹµŃéŗóµÄ¼ĒĀ¼£ŗ
¢ŁZnĪŖÕż¼«£¬CuĪŖøŗ¼«
¢ŚCu¼«ÉĻÓŠĘųÅŻ²śÉś£¬·¢Éś»¹Ō·“Ó¦
¢ŪSO42©ĻņZn¼«ŅʶÆ
¢ÜČōÓŠ0.5molµē×ÓĮ÷¾µ¼Ļߣ¬Ōņ²śÉś5.6LĘųĢå
¢ŻĶāµēĀ·µēĮ÷µÄĮ÷ĻņŹĒ£ŗCu”śZn
¢Žøŗ¼«·“Ó¦Ź½£ŗCu©2e©ØTCu2+£¬·¢ÉśŃõ»Æ·“Ó¦
A. ¢Ś¢Ü¢Ż B. ¢Ś¢Ū¢Ż C. ¢Ł¢Ü¢Ž D. ¢Ś¢Ū¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com