
| A. | 电解食盐水若产生2g氢气,则转移的电子数目为NA | |
| B. | 电解精炼铜时转移0.1 NA个电子,则阳极溶解3.2g铜 | |
| C. | VL amol/L FeCl3 溶液中,若Fe3+数目为NA,则Cl-的数目大于3NA | |
| D. | 100mL 1mol/L的醋酸溶液中,CH3COO-离子数为0.1NA |
分析 A.依据电解饱和食盐水电解反应和电子守恒计算分析;
B.粗铜中含有杂质铁、锌等活泼金属,电解过程中优先放电,所以阳极溶解的铜减少;
C.铁离子在溶液中发生水解,导致铁离子数目减少,氯离子的数目大于铁离子数目的3倍;
D.醋酸为弱电解质,溶液中只能部分电离出醋酸根离子;
解答 解:A.电解食盐水若产生2g氢气,物质的量=$\frac{2g}{2g/mol}$=1mol,电解反应为2H++2e-=H2↑,则转移的电子数目为2NA,故A错误;
B.电解精炼铜时转移0.1NA个电子,转移了0.1mol电子,由于粗铜中杂质铁、锌优先放电,所以阳极减少的铜的物质的量小于0.05mol,减少的质量小于3.2g,故B错误;
C.VL a mol/L FeCl3溶液中,铁离子部分水解,溶液中铁离子数目减少,若Fe3+数目为NA,则Cl-的数目大于3NA,故C正确;
D.100mL 1mol/L的醋酸溶液中含有溶质醋酸0.1mol,醋酸为弱电解质,0.1mol醋酸电离出的醋酸根离子小于0.1mol,所以溶液中CH3COO-离子数小于0.1NA,故D错误;\
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,注意粗铜中含有活泼性较强的铁、锌等杂质;试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④ | C. | ①② | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | a+n=b-m | B. | X的氢化物化学式为HnX或XHn | ||
| C. | a<b | D. | Y的氧化物化学式为YOm |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1mol CO、2mol H2 | 1mo l CH3OH | 2mol CH3OH | |
| 平衡时数据 | CH3OH的 浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO是一种红棕色气体 | |
| B. | NO2与水反应生成硝酸,所以NO2是硝酸的酸酐 | |
| C. | NO和NO2是引发光化学烟雾的主要污染源 | |
| D. | NO2可用排水法收集 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
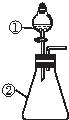 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选項 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 氢氧化钠稀溶液 | 硫酸铝铵溶液 | 立即产生白色沉淀 |
| B | 氢氧化钠浓溶液 | 用砂纸打磨过的镁条 | 立即产生大量无色气体 |
| C | 浓硫酸 | 铜粉 | 立即产生刺激性气味气体 |
| D | 盐酸 | 较浓的硝酸亚铁溶液 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
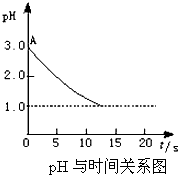 某课题小组的同学对“电解氯化铜溶液时的pH变化”的问题,有以下两种不同的观点:
某课题小组的同学对“电解氯化铜溶液时的pH变化”的问题,有以下两种不同的观点:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com