
| 选项 | 物质或离子 | 能否共存 | 原因解释 |
| A | 常温常压下:NH3、O3、H2、HCl | 不能共存 | NH3为碱性气体,HCl为酸性气体,发生的反应为:NH3+HCl=NH4Cl |
| B | 水溶液中:K+、Ag+、NO3-、NH3•H2O | 不能共存 | 发生反应的离子方程式为:Ag++OH-=AgOH↓ |
| C | 水电离出的c(OH-)=1×10-13mol/L的溶液中:Fe2+、MnO4-、SO42-、Na+ | 不能共存 | 只可能发生反应:Fe2++2OH-=Fe(OH)2↓ |
| D | 溶液中:Al3+、Na+、SO42-、CO32- | 可以共存 | 不能发生反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.常温下NH3、HCl发生化合反应;
B.Ag+、NH3•H2O生成沉淀,NH3•H2O在离子反应中保留化学式;
C.水电离出的c(OH-)=1×10-13mol/L的溶液,为酸或碱溶液;
D.离子之间相互促进水解.
解答 解:A.常温下NH3、HCl发生化合反应,是因NH3为碱性气体,HCl为酸性气体,发生的反应为:NH3+HCl=NH4Cl,则不能大量共存,故A正确;
B.Ag+、NH3•H2O生成沉淀,NH3•H2O在离子反应中保留化学式,离子反应为Ag++NH3•H2O=AgOH↓+NH4+,故B错误;
C.水电离出的c(OH-)=1×10-13mol/L的溶液,为酸或碱溶液,酸性溶液中Fe2+、MnO4-发生氧化还原反应,故C错误;
D.Al3+、CO32-相互促进水解,不能大量共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、相互促进水解反应、氧化还原反应的离子共存考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
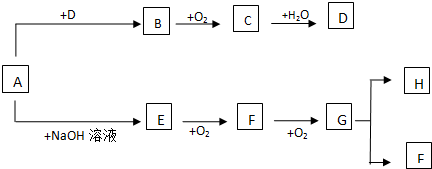
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
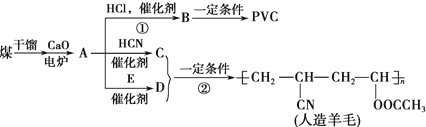
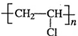 ,CH2C=HC-CN.
,CH2C=HC-CN.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
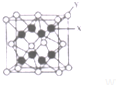 A~E五种元素均位于周期表的前四周期,有关它们的信息如下表所示:
A~E五种元素均位于周期表的前四周期,有关它们的信息如下表所示:| 元素 | 相关信息 |
| A | 元素A是周期表中原子半径最小的元素 |
| B | B的单质由双原子分子构成,分子中有14个电子 |
| C | C3单质在大气层的平流层中,其浓度的减少会导致人患皮肤癌 |
| D | D是前四周期元素中第一电离能最小的元素 |
| E | E位于ds区且原子的最外层电子数与A相同 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
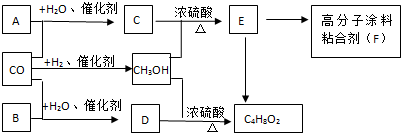
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | a中试剂 | b中试剂 | 实验现象 | 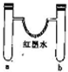 |
| A | 1mL12mol•L-1浓盐酸0.5gMnO2 | 0.1gCaCO3、1mL 2mol•L-1盐酸 | 红墨水褪色,U形管中液面左右基本持平 | |
| B | 0.1gNa3mol水 | 0.1gNa 3mol乙醇 | 反应开始阶段,反应结束静置一段时间后U形管中液面都是左低右高 | |
| C | 3mL浓硫酸、铁钉 | 3mLNaCl溶液、铁钉 | 铁钉均生锈,U形管中液面左高右低 | |
| D | 3mL水 | 3mL饱和FeSO4溶液 | 一段时间后,U形管中液面左低右高,b管溶液中出现红褐色浑浊物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
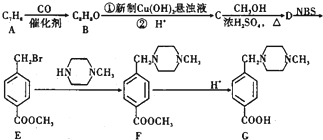
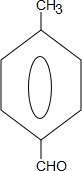

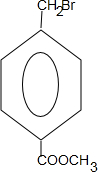 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$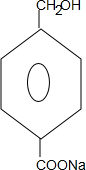 +CH3OH+NaBr
+CH3OH+NaBr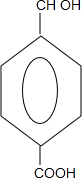 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$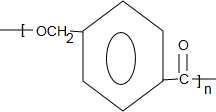 +nH2O
+nH2O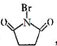 ,则关于NBS与D反应生成E的 说法错误的是 ( )
,则关于NBS与D反应生成E的 说法错误的是 ( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com