
【题目】能证明氢氟酸是弱酸的实验事实是
A.HF溶液与Zn反应放出H2
B.0.1mol/LNaF溶液的pH大于7
C.HF溶液与Na2CO3反应生成CO2
D.0.1mol/LHF溶液可使紫色石蕊变红
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g/mL,沸点约55 oC,分离水和丙酮时最合理的方法是
A. 蒸发 B. 分液 C.过滤 D. 蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)达到平衡状态,其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)达到平衡状态,其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K[来 | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= ;再充入CO2气体,则平衡 移动(选“正向移动”、“逆向移动”或“不移动”),平衡常数K (选“增大”、“减小”或“不变”)。
(2)该反应的逆反应方向为 反应方向(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下的各物质平衡浓度符合:c(CO2)=c(CO),c(H2)=c(H2O),试判断此时的温度为 ℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种优质燃料,在工业上常用CO和H2合成甲醇,反应方程式为CO(g)+2H2(g) =CH3OH(g)。
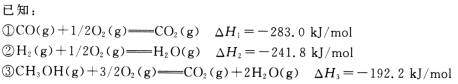
(1)计算CO(g)+2H2(g)=CH3OH(g)的反应热△H4=____________。
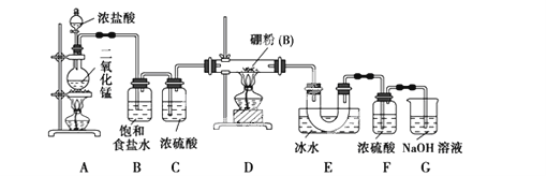
(2)为了提高燃料的利用率可以将甲醇设计为燃料电池,并用以此为电源进行电解实验,装置如图所示,回答相关问题。
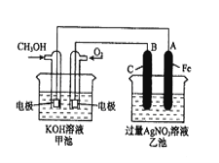
①写出通甲醇一极的电极反应方程式 ;写出乙池中B(C)电极的电极反应式 ;
②反应过程中,乙池溶液pH的变化为 (升 高、降低或不变)
③当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,下列说法不能表明反应A(s)+2B(g)![]() C(g)+D(g)已达平衡的是( )
C(g)+D(g)已达平衡的是( )
A.B的物质的量浓度 B.混合气体的压强不变
C.混合气体的密度 D.混合气体的相对分子质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是
A.向水中投入一小块金属钠 B.向水中通入二氧化硫气体
C.将水加热煮沸 D.向水中加硫酸钠晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是
A.使用催化剂,可加快反应速率,目的是提高生产效率
B.使用冰箱保存食物,是利用了化学反应速率理论
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使用有限原料多出产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可由乙苯生产苯乙烯和氢气,下列说法不正确的是
A. 乙苯的同分异构体共有三种
B. 该反应的类型为消去反应
C. 可用Br2/CCl4鉴别乙苯和苯乙烯
D. 苯乙烯分子中共平面的碳原子数最多为8个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2(g)与H2(g)在铁催化剂表面经历如下过程生成NH3(g):
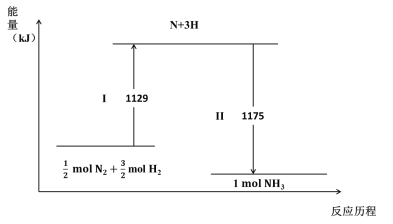
下列说法不正确的是
A.Ⅰ过程中破坏的均为非极性键
B.Ⅰ过程吸收能量,II过程放出能量
C. N2(g) + 3H2(g) ![]() 2NH3(g) ΔH = –44 kJ·mol-1
2NH3(g) ΔH = –44 kJ·mol-1
D.1mol N2(g)与3 mol H2(g)所具有的总能量比2 mol NH3(g) 所具有的总能量高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com