
| A. | 在溴乙烷中直接加入AgNO3溶液 | |
| B. | 加蒸馏水,充分搅拌后,加入AgNO3溶液 | |
| C. | 加入NaOH的乙醇溶液,加热后加入AgNO3溶液 | |
| D. | 加入NaOH溶液加热,冷却后加入稀硝酸酸化,然后加入AgNO3溶液 |
分析 先将溴乙烷中的溴元素转化为溴离子,硝酸银和溴离子反应生成不溶于酸的浅黄色沉淀,所以再用硝酸银溶液检验溴离子是否存在,从而证明溴乙烷中是否含有溴元素.
解答 解:在NaOH水溶液中加热,溴乙烷水解脱掉-Br生成Br-,再加HNO3酸化(NaOH过量,下一步加的Ag+会和OH-反应变成不稳定的AgOH,近而变成白色沉淀Ag2O,影响实验,所以加H+把OH-除掉),再加AgNO3溶液,如果生成浅黄色沉淀,则证明溴乙烷中含有溴元素,
故选D.
点评 本题考查物质的检验和鉴别的设计,侧重于学生的分析能力和实验能力的考查,易错点为卤代烃水解是碱性溶液中进行或在在氢氧化钠醇溶液中发生消去反应,加硝酸银时必须先加酸中和碱才能出现溴化银沉淀,注意实验的操作步骤.


科目:高中化学 来源: 题型:选择题
| A. | 恒温恒容容器中发生反应C(s)+H2O(g)?CO(g)+H2(g),当混合气体密度不变时反应达到平衡 | |
| B. | 平衡向右移动时,反应物的转化率一定增大,平衡常数不一定增大 | |
| C. | 恒温时向BaSO4悬浊液中加入Na2SO4固体,Ba2+浓度减小,溶度积KsP (BaSO4)不变 | |
| D. | 向氨水中逐滴加入盐酸,溶液呈中性时离子浓度为:c(Cl-)═c(NH4+)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 编号 | T/K | 催化剂的用量/g | 酸性KMnO4溶液的浓度/mol•L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a.实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; b.实验①和③探究温度对该反应速率的影响; c.实验①和④探究催化剂对该反应速率的影响. |
| ② | 298 | 0.5 | 0.0010 | |
| ③ | 323 | 0.5 | 0.010 | |
| ④ | 298 | 0 | 0.010 |
| 实验编号 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| ① | 14.0 | 13.0 | 11.0 |
| ② | 6.0 | 7.0 | 7.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2和NaOH溶液 | B. | NH3和稀盐酸 | C. | NO2和水 | D. | SO2和NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 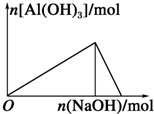 向AlCl3溶液中滴加NaOH溶液 | B. |  向NaOH溶液中滴加AlCl3溶液 | ||
| C. | 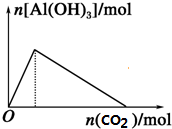 向NaAlO2溶液中滴加CO2 | D. |  向AlCl3溶液中滴氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
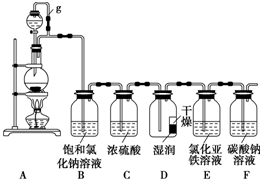
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
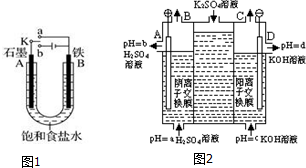
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com