
| 应称取氢氧化钠固体的质量/g | 应选用容量瓶的规格/mL | 除烧杯、托盘天平、容量瓶、量筒外还需的其它仪器 |
| 10.0 | 250 | 玻璃棒、胶头滴管、药匙 |
分析 (1)利用n=cV计算出氢氧化钠的物质的量,再根据m=nM计算所需氢氧化钠的质量;根据配制240mL氢氧化钠溶液应选250mL容量瓶;根据配制溶液的操作步骤选择所用仪器;
(2)据配制溶液的实验操作过程进行实验步骤排序;
(3)依据根据容量瓶的使用方法和规则来回答;
(4)根据公式c=n/V,可以根据影响n和V的因素来分析回答;
(5)分析操作对溶质的物质的量、溶液的体积的影响,作出判断.
解答 解:(1)依据物质的量的关系n=cV=1×0.25=0.25mol,m=nM=0.25mol×40g/mol=10.0g;根据配制240mL氢氧化钠溶液应选250mL容量瓶;根据配制溶液的操作步骤选择所用仪器,除烧杯、托盘天平、容量瓶、量筒外还需玻璃棒、胶头滴管、药匙,
故答案为:10.0,250,玻璃棒、胶头滴管、药匙;
(2)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,所以配制时,其正确的操作顺序是BCAFED,
故答案为:B、C、A、F、E、D;
(3)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶,减少误差,容量瓶盛放热溶液时,液体热胀冷缩,会导致体积不准,并且也易导至容量瓶炸裂,
故答案为:保证溶质全部转入容量瓶;容量瓶盛放热溶液时,体积不准,也易导至容量瓶炸裂;
(4)根据c=n/v可知,凡是能够使n偏小或者使V偏大的操作都会是溶液的浓度偏小,反之,溶液的浓度偏大;没有进行A操作,导致溶质的物质的量偏小,配制溶液的浓度偏低;加蒸馏水时不慎超过了刻度,导致溶液的体积偏大,配制溶液的浓度偏低;定容时俯视偏低,导致溶液的体积偏小,配制溶液的浓度偏高,
故答案为:偏低,偏低,偏高;
(5)加蒸馏水时不慎超过了刻度线,实验失败,无法挽回,必须重新配置;向容量瓶中转移溶液时不慎有溶液溅出,溶质的物质的量不准确,实验失败,必须重新配置;
故答案为:宣告实验失败,洗净容量瓶后重新配制;宣告实验失败,洗净容量瓶后重新配制.
点评 本题考查了配制一定物质的量浓度的溶液方法,题目难度不大,注意掌握配制一定物质的量浓度的溶液方法及容量瓶的选取方法,明确误差分析的方法与技巧.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 强电解质溶液的导电能力一定比弱电解质强 | |
| B. | 冰醋酸是弱电解质,但液态时不能导电 | |
| C. | 盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱 | |
| D. | 硫酸钠是强电解质,硫酸钡是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同周期元素的原子半径以ⅦA族的最大 | |
| B. | 同主族两种元素原子的核外电子数的差值可能为36 | |
| C. | 短周期中次外层电子数是最外层电子数2倍的原子一定是非金属元素的原子 | |
| D. | 科学家在周期表中金属与非金属分界线处找到了优良的催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
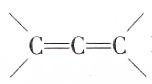 不稳定).
不稳定).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | pH=2的HA酸溶液与pH=12的MOH碱溶液以任意比混合:c(OH-)+c(M+)=c(H+)+c(A-) | |
| B. | 将物质的量浓度均为0.1mol•L-1的Na2CO3溶液和NaHCO3溶液等体积混合所得溶液中:2c(OH-)-2c(H+)=3c(H2CO3)+c(HCO${\;}_{3}^{-}$)-c(CO${\;}_{3}^{2-}$) | |
| C. | 等浓度、等体枳的Na2CO3和NaHCO3混合:$\frac{c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$<$\frac{c(C{O}_{3}^{2-})}{c(HC{O}_{3}^{-})}$ | |
| D. | 将足量AgCl分别放入:①5mL水,②10mL0.2mol/LMgCl2,③20mL0.3mol/L盐酸中溶解至饱和,c(Ag+):①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | HA 物质的量 | NaOH 物质的量 | 混合后溶 |
| 编号 | 浓度/(mol•L-1) | 浓度/(mol•L-1) | 液的 pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol/L KCl溶液 | B. | 自来水 | ||
| C. | 0.5mol/L盐酸 | D. | 0.5mol/L醋酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁杵成针 | B. | 抱薪救火 | C. | 闭门造车 | D. | 刻舟求剑 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com