
【题目】磷矿石的主要成分是Ca5F(PO4)3,并含有少量MgO、Fe2O3等杂质。工业上以磷矿石为原料制备H3PO4,一种生产流程如下:

已知:Ca5F(PO4)3 + 7H3PO4→5Ca(H2PO4)2 + HF
38、写出有关操作的名称:Ⅰ___________、Ⅲ_________。工艺流程中设计操作Ⅱ与Ⅲ的目的是__________________________________。
39、若在实验室里采用此种方法溶解磷矿石,请写出必须的实验注意事项,并说明理由:_____________。
40、磷矿石也可直接用硫酸溶解,两种工艺相比,该工艺的优点是____________________。
41、测定产品磷酸的浓度可采用滴定法。准确量取10.00 mL磷酸产品(密度为1.526g/cm3)溶于水配成1L溶液;取稀释后的溶液20.00mL,以甲基橙为指示剂,用0.103 mol/L标准NaOH溶液滴定;当观察到溶液恰好变色,且在半分钟内不变色,即为滴定终点(生成NaH2PO4),消耗标准溶液20.16 mL。
该实验过程中需要的定量仪器有______________________________(写名称)。
42、若理论上滴定应耗用标准溶液20.20 mL,则相对误差为______________(按近似计算法则)。该产品中磷酸的质量分数为_____________(保留3位小数)。
【答案】过滤 萃取 除去磷酸粗品中的杂质Mg2+、Fe3+等 不能使用玻璃器皿,因为HF会腐蚀玻璃。或要在密闭系统中进行,因为HF有剧毒 避免生成的石膏沉积在磷矿石表面,阻碍反应顺利进行 滴定管 1000 mL容量瓶 -0.2% 0.667
【解析】
磷矿石的主要成分是Ca5F(PO4)3,并含有少量MgO、Fe2O3等杂质,磷矿石加入稀磷酸溶解生成磷酸二氢钙和氟化氢,加入硫酸沉淀除除氟,过滤得到彻底石膏,滤液为磷酸粗品,磷酸粗品中含有H+、Ca2+、Mg2+、Fe3+离子,加入萃取剂萃取,分液后再加入水反萃取,用来除去磷酸粗品中的杂质Mg2+、Fe3+等,得到溶液浓缩得到较纯净的磷酸;
(1)操作Ⅰ通过过滤分离出石膏,根据图示,磷酸粗品中含有H+、Ca2+、Mg2+、Fe3+离子,操作Ⅱ、Ⅲ是萃取和反萃取,用来除去磷酸粗品中的杂质Mg2+、Fe3+等;
(2)HF具有腐蚀性,能够腐蚀玻璃,不能使用玻璃仪器溶解磷矿石;
(3)直接用硫酸溶解磷矿石,生成的石膏会沉积在磷矿石表面;
(3)根据萃取操作用到的仪器完成;根据萃取操作中对萃取剂要求分析;
(4)定量仪器是准确量取溶液的滴定管,配制1L溶液的容量瓶;
(5)相对误差= ![]() ×100%,根据生成产物NaH2PO4和氢氧化钠的关系式及滴定数据,计算出磷酸产品的质量分数。
×100%,根据生成产物NaH2PO4和氢氧化钠的关系式及滴定数据,计算出磷酸产品的质量分数。
38.操作Ⅰ通过过滤分离出石膏,根据图示,磷酸粗品中含有H+、Ca2+、Mg2+、Fe3+离子,操作Ⅱ、Ⅲ是萃取和反萃取,萃取时,必须满足萃取剂与水互不相溶、萃取的物质在水中的溶解度较小,工艺流程中设计操作Ⅱ与Ⅲ的目的是用来除去磷酸粗品中的杂质Mg2+、Fe3+等;
故答案为:过滤;萃取;除去磷酸粗品中的杂质Mg2+、Fe3+等;
39.若在实验室里采用此种方法溶解磷矿石,由于HF具有腐蚀性,能够腐蚀玻璃,所以不能使用玻璃仪器,或要在密闭系统中进行,因为HF有剧毒;
故答案为:不能使用玻璃器皿,因为HF会腐蚀玻璃或要在密闭系统中进行,因为HF有剧毒;
40.如果直接用硫酸溶解磷矿石,生成的石膏会沉积在磷矿石表面,该工艺避免了生成的石膏沉积在磷矿石表面;
故答案为:避免生成的石膏沉积在磷矿石表面;
41.准确量取10.00mL磷酸产品(密度为1.526g/cm3)溶于水配成1L溶液;取稀释后的溶液20.00mL,以甲基橙为指示剂,用0.103mol/L标准NaOH溶液滴定,该实验过程中需要的定量仪器有准确量取溶液的滴定管,配制溶液所需的1000mL的容量瓶;
故答案为:滴定管、1000mL容量瓶;
42.相对误差=![]() ×100%=
×100%=![]() ×100%=-0.2%;磷酸产品的质量是:10.00mL×1.526g/cm3=15.26g,1L磷酸产品配成的溶液消耗0.103mol/L标准NaOH溶液的体积为:20.16mL×
×100%=-0.2%;磷酸产品的质量是:10.00mL×1.526g/cm3=15.26g,1L磷酸产品配成的溶液消耗0.103mol/L标准NaOH溶液的体积为:20.16mL×![]() =1.008L,磷酸与氢氧化钠反应的关系式为:H3PO4~NaH2PO4~NaOH,n(H3PO4)=n(NaOH)=0.103mol/L×1.008L≈0.1040mol,所以该磷酸产品的质量分数为:
=1.008L,磷酸与氢氧化钠反应的关系式为:H3PO4~NaH2PO4~NaOH,n(H3PO4)=n(NaOH)=0.103mol/L×1.008L≈0.1040mol,所以该磷酸产品的质量分数为:![]() ×100%≈66.7%;
×100%≈66.7%;
故答案为:-0.2%;66.7%。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】“84消毒液”是生活中常用的消毒剂,可与硫酸溶液反应制取氯气,反应原理为NaClO+NaCl+H2SO4![]() Na2SO4+Cl2↑+H2O。为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置:
Na2SO4+Cl2↑+H2O。为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置:
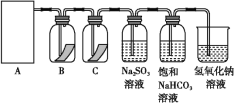
(1)从①、②、③装置中选择合适的制氯气装置(A处)______(填写序号)。
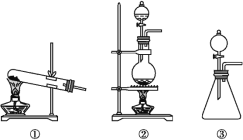
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是________________;说明该装置存在明显的缺陷,请提出合理的改进方法:________________。
(3)为了验证氯气的氧化性,将氯气通入Na2SO3溶液中,反应的离子方程式为_____,然后检验反应后溶液中是否含有S![]() 。检验S
。检验S![]() 的方法是:取少量反应后的溶液于试管中,先加入足量的________________至无明显现象,然后再加入少量____溶液,有白色沉淀生成,说明含有S
的方法是:取少量反应后的溶液于试管中,先加入足量的________________至无明显现象,然后再加入少量____溶液,有白色沉淀生成,说明含有S![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:
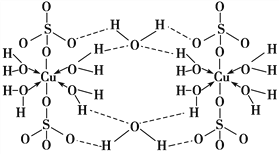
下列有关胆矾的说法正确的是( )
A. 所有氧原子都采取sp3杂化 B. 氧原子参与形成配位键和氢键两种化学键
C. Cu2+的价电子排布式为3d84s1 D. 胆矾中的水在不同温度下会分步失去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是进行Mg与SiO2反应的实验装置,O2和H2O(g)的存在对该实验有较大影响。

下列说法不正确的是
A.装稀硫酸仪器的名称是分液漏斗,II中洗气瓶内是碳酸氢钠溶液
B.可以把装置I换成启普发生器
C.实验开始时,必须先通一段时间X气体,再在III处加热
D.当III处反应引发后,移走酒精灯,反应仍进行,说明该反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、N及S的化合物用途非常广泛。回答下列问题;
(1)基态Fe原子价电子排布图为____;基态S原子的核外电子占据最高能级的电子云轮廓图为__________形。
(2)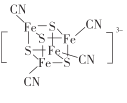 团簇离子中,Fe2+、Fe3+数目之比为______;与铁形成配位键的原子是________,铁的配位数为_________。
团簇离子中,Fe2+、Fe3+数目之比为______;与铁形成配位键的原子是________,铁的配位数为_________。
(3)四氟铵可通过下列反应制备:NF3+F2 + BF3 =NF4 BF4
①NF3的空间构型为_____ , 中心原子的杂化方式是______。
②NF4BF4存在的作用力有________(填字母)。
A. σ键 B. π键 C.离子键. D.配位键
(4)Fe与S形成的一种化合物晶体的结构如图所示,六棱柱底边边长为a pm,高为c pm,阿伏加德罗常数的值为NA,该Fe、S化合物晶体的密度为_____(列出计算式)g. cm-3
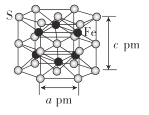
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果。只改变一个条件,则下列对图像的解读正确的是
①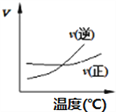 ②
②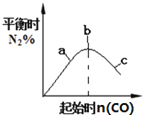 ③
③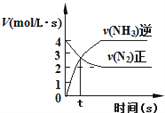 ④
④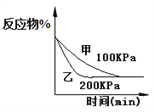
A. A2(g)+3B2(g)![]() 2AB3(g),如图①说明此反应的正反应是吸热反应
2AB3(g),如图①说明此反应的正反应是吸热反应
B. 4CO(g)+2NO2(g)![]() N2(g)+4CO2(g),如图②说明NO2的转化率b>a>c
N2(g)+4CO2(g),如图②说明NO2的转化率b>a>c
C. N2(g)+3H2(g)![]() 2NH3(g),如图③说明t秒时合成氨反应达到平衡
2NH3(g),如图③说明t秒时合成氨反应达到平衡
D. 2A(g)+2B(g)![]() 3C(g)+D(?),如图④说明生成物D一定是气体
3C(g)+D(?),如图④说明生成物D一定是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚被称为21世纪的新型燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上常采用甲醇气相脱水法来获取。其反应方程式为:2CH3OH(g)![]() CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
完成下列填空:
28、有机物分子中都含碳元素,写出碳原子最外层电子的轨道表示式_______________;
写出甲醇分子中官能团的电子式_________________。
29、碳与同主族的短周期元素相比,非金属性较强的是_________(填元素符号)。写出一个能证明你的结论的化学方程式_____________________________________。
30、在温度和体积不变的情况下,能说明反应已达到平衡状态的是______(选填编号)
a.CH3OH的消耗速率与CH3OCH3的消耗速率之比为2:1
b.容器内压强保持不变
c.H2O(g)浓度保持不变
d.气体平均相对分子质量保持不变
31、一定温度下,在三个体积约为2.0 L的恒容密闭容器中发生上述反应:
容器 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.40 | 0.16 | 0.16 |
Ⅱ | 387 | 0.80 | a | |
Ⅲ | 207 | 0.40 | 0.18 | 0.18 |
(1)若要提高CH3OH的平衡转化率,可以采取的措施是______(选填编号)。
a.及时移走产物 b.升高温度 c.充入CH3OH d.降低温度
(2)I号容器内的反应经过t min达到平衡,则CH3OH的平均反应速率为_____________(用含t的式子表示)。II号容器中a =___________mol。
32、若起始时向容器I中充入CH3OH 0.2mol、CH3OCH3 0.30mol和H2O 0.20mol,则反应将向__________(填“正”“逆”)反应方向进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学固氮可以在常温常压下实现氮气的还原合成氨,某课题组提出一种全新的电化学固氮机理——表面氢化机理示意图如下,则有关说法错误的是
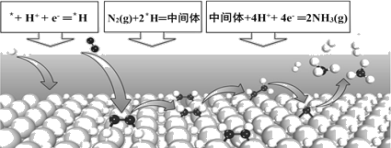
A.在表面氢化机理中,第一步是H+的还原反应
B.在表面*H原子与催化剂的协同作用下,N2与表面*H原子反应生成*N2H4中间体
C.电化学固氮法较传统工业合成氨法,具有能耗小、环境友好的优点
D.若竞争反应(析氢反应)的活化能显著低于固氮反应,则析氢反应的速率要远远高于固氮反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氮原子的最外层电子排布式是__;氮元素有多种化合价,列举一例含二种氮元素化合价的化合物__。
(2)肼(N2H4)分子可视为NH3分子的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。NH3分子的空间构型是__;与N2H4分子具有相同电子数的分子有多种,其中具有可燃性的物质是__(化学式)。
(3)肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)→3N2(g)+4H2O(g)+1038.7kJ,若该反应中有4molN-H键断裂,则形成的气体有__mol,其中转移电子数为__。
(4)肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__(填标号)
a.离子键 b.共价键 c.金属键 d.范德华力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com