
| 阶段/含量%/成分 | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| 预处理前 | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| 预处理后 | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
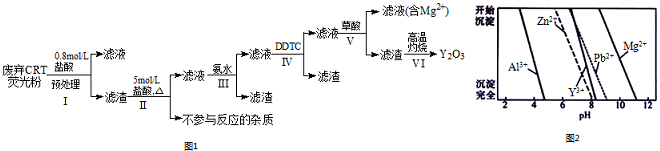
分析 废弃CRT荧光粉的化学组成为Y2O3、ZnO、Al2O3、PbO2、MgO等,加盐酸,过滤,滤渣主要含有Y2O3,还有少量的PbO2、ZnO、Al2O3、MgO,再加5mol/L的盐酸,PbO2与HCl发生氧化还原反应,生成氯气和PbCl2,Y2O3转化为Y3+,过滤,滤液中含有Pb2+和Y3+、Al3+、Zn2+、Mg2+,再加氨水,Al3+形成Al(OH)3沉淀,过滤,滤液中含有Pb2+和Y3+、Zn2+、Mg2+,加DDTC除去溶液中的Pb2+和Zn2+,过滤,滤液中加草酸,生成Y2(C2O4)3沉淀,过滤,滤渣为Y2(C2O4)3固体,高温灼烧Y2(C2O4)3生成Y2O3;
(1)进行原料预处理可以除去部分ZnO和Al2O3,富集稀土元素等;
(2)PbO2与HCl发生氧化还原反应,生成氯气和PbCl2,根据原子守恒和得失电子守恒写出方程式;
(3)步骤Ⅲ是用氨水除去溶液中的Al3+;
(4)根据流程分析;由图2可知Zn2+、Pb2+与Y3+沉淀的pH相近;
(5)根据Ksp[Y2(C2O4)3]=c2(Y3+)×c3(C2O42-)计算;
(6)草酸钇隔绝空气加热可以得到Y2O3和CO、CO2.
解答 解:废弃CRT荧光粉的化学组成为Y2O3、ZnO、Al2O3、PbO2、MgO等,加盐酸,过滤,滤渣主要含有Y2O3,还有少量的PbO2、ZnO、Al2O3、MgO,再加5mol/L的盐酸,PbO2与HCl发生氧化还原反应,生成氯气和PbCl2,Y2O3转化为Y3+,过滤,滤液中含有Pb2+和Y3+、Al3+、Zn2+、Mg2+,再加氨水,Al3+形成Al(OH)3沉淀,过滤,滤液中含有Pb2+和Y3+、Zn2+、Mg2+,加DDTC除去溶液中的Pb2+和Zn2+,过滤,滤液中加草酸,生成Y2(C2O4)3沉淀,过滤,滤渣为Y2(C2O4)3固体,高温灼烧Y2(C2O4)3生成Y2O3;
(1)由表格数据可知:进行原料预处理可以除去部分ZnO和Al2O3,富集稀土元素;在后续操作中能降低耗酸量等,
故答案为:除去ZnO和Al2O3;富集稀土元素;降低后续耗酸量等;
(2)PbO2与HCl发生氧化还原反应,生成氯气和PbCl2,则反应的方程式为:PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O,
故答案为:PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O;
(3)由流程分析可知,步骤Ⅲ是用氨水除去溶液中的Al3+,其反应的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(4)根据流程分析可知,步骤Ⅳ中除杂试剂DDTC除去的杂质离子有;由图2可知Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离,所以不能通过直接加碱的方法除去Zn2+、Pb2+;
故答案为:Zn2+、Pb2+;Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离;
(5)已知:当离子浓度小于10-5mol/L时,沉淀就达完全,Ksp[Y2(C2O4)3]=c2(Y3+)×c3(C2O42-)=(10-5)2×c3(C2O42-)=8.0×10-28,则c(C2O42-)=$\root{3}{\frac{8.0×10{\;}^{-28}}{(10{\;}^{-5}){\;}^{2}}}$=2.0×10-6mol/L,故答案为:2.0×10-6;
(6)草酸钇隔绝空气加热可以得到Y2O3和CO、CO2,其反应的方程式为Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑,
故答案为:Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑.
点评 本题考查了物质的分离提纯实验操作,题目涉及到氧化还原、出除杂质、溶度积常数的应用等,题目难度中等,注意根据题意写出有关反应的方程式,做题时注意根据物质的性质正确判断反应物和生成物,用守恒的方法去书写.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
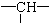 ,其余为氯原子.则氯原子的个数为( )
,其余为氯原子.则氯原子的个数为( )| A. | 2y+3x-x | B. | z+2-x | C. | 2y+z-x | D. | z+2y+2-x |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.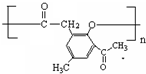 .
.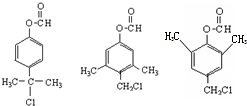 .
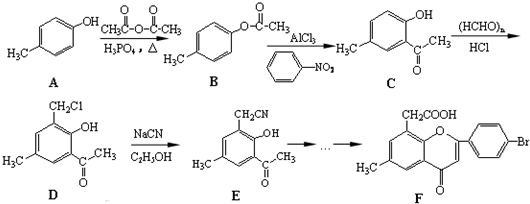
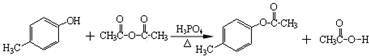
.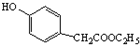 )是一种重要的医药中间体.写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
)是一种重要的医药中间体.写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选).合成路线流程图示例如下: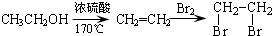
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2 H2O | B. | NH3 BCl3 | C. | PCl3 CH4 | D. | PCl5 CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
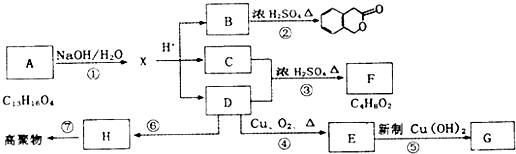
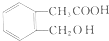
 ④
④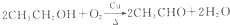 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
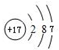 .
.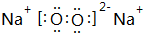 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100ml 2mol/LFeCl3溶液 | B. | 75ml 1mol/LMgCl2溶液 | ||
| C. | 150ml 3mol/LKCl溶液 | D. | 25ml 2mol/LAlCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com