
【题目】在容积为2L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示200 ℃、100 ℃下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示200 ℃、100 ℃下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
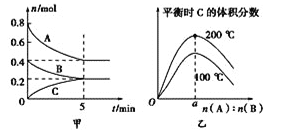
A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04mol·L-1·min-1
B. 若在图甲所示的平衡状态下再向体系中充入He,此时v正> v逆
C. 由图乙可知,反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=1
zC(g)的ΔH<0,且a=1
D. 200℃时,向容器中充入2molA和1molB,达到平衡时A的体积分数小于0.5
【答案】D
【解析】
A. 由图甲可知,200℃时5min达到平衡,平衡时B的物质的量变化量为△n(B)=0.4mol-0.2mol=0.2mol,则v(B)=![]() =0.02 mol·L-1·min-1,故A错误;
=0.02 mol·L-1·min-1,故A错误;
B.恒温恒容条件下通入氦气,反应混合物的浓度不变,平衡不移动,则v正=v逆,故B错误;
C.由图乙可知,n(A):n(B)一定时,温度越高平衡时C的体积分数越大,说明升高温度平衡向正反应方向移动,升高温度平衡向吸热反应方向移动,故正反应为吸热反应,即△H>0;由图甲可知,200℃达到平衡时,A的物质的量变化量为△n(A)=0.8mol-0.4mol=0.4mol,B的物质的量变化量为0.2mol,在一定温度下只要A、B起始物质的量之比恰好等于化学方程式中化学计量数之比,平衡时生成物C的体积分数就最大,A、B的起始物质的量之比=0.4mol:0.2mol=2,即a=2,故C错误;
D.由图甲可知,200℃达到平衡时,A、B、C的物质的量变化量分别为0.4mol、0.2mol、0.2mol,物质的量变化量之比等于化学计量数之比,故x:y:z=0.4mol:0.2mol:0.2mol=2:1:1,平衡时A 的体积分数为![]() =0.5,200℃时,向容器中充入2 mol A 和1 mol B达到的平衡状态相当于在原平衡基础上增大压强,平衡正向移动,则达到平衡时,A 的体积分数小于0.5,故D正确,答案选D。
=0.5,200℃时,向容器中充入2 mol A 和1 mol B达到的平衡状态相当于在原平衡基础上增大压强,平衡正向移动,则达到平衡时,A 的体积分数小于0.5,故D正确,答案选D。


科目:高中化学 来源: 题型:
【题目】某草酸二酯结构简式如图,下列说法正确的是

A. 草酸二酯的分子式为C26H22Cl6O8
B. 1mol草酸二酯与氢氧化钠稀溶液反应时(苯环上卤素不水解),最多消耗4molNaOH
C. 草酸二酯能发生的反应类型有氧化、还原、取代、加成、聚合、酯化
D. 草酸二酯酸性条件下充分水解可以得到三种有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温密闭容器中发生反应:CaCO3(s)![]() CaO(s)+CO2(g) H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是
CaO(s)+CO2(g) H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是

A. υ逆(逆反应速率) B. ρ(容器内气体密度)
C. m(容器内CaO质量) D. Qc(浓度商)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一个绝热恒容密闭容器中通入CO(g)和H2O(g),一定条件下使反应CO(g)+H2O(g)![]() CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是
CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是
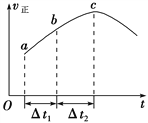
A. 反应物浓度:a点小于c点
B. 该反应的正反应为放热反应
C. c点达到平衡状态
D. Δt1=Δt2时,H2的产率:a~b段大于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定温度下,X(g)+2Y(g)![]() mZ(g);ΔH =-akJ/mol(a>0)现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达平衡状态时,放出热量bkJ;向密闭容器乙中通入2molX和4molY,达平衡状态时,放出热量ckJ,且2b < c,则下列各值关系正确的是
mZ(g);ΔH =-akJ/mol(a>0)现有甲、乙两容积相等且固定的密闭容器,在保持该温度下,向密闭容器甲中通入1molX和2molY,达平衡状态时,放出热量bkJ;向密闭容器乙中通入2molX和4molY,达平衡状态时,放出热量ckJ,且2b < c,则下列各值关系正确的是
A. a = b B. 2a < c C. m > 3 D. m < 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 Cl2 通入 NaBr 和 NaI 的混合液中,待反应充分后将所得的溶液加热蒸干,并灼烧,最后将得 到的固体冷却、称量.称量所得固体的质量与通入 Cl2 的体积关系如图所示.则原混合液中 NaI 的物 质的量为( )

A. 0.5 mol B. 0.4 mol C. 0.3 mol D. 0.25 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
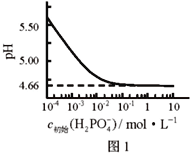
【题目】LiH2PO4是制备电池的重要原料。室温下,LiH2PO4溶液的pH随c初始(H2PO4–)的变化如图1所示,H3PO4溶液中H2PO4–的分布分数![]() 随pH的变化如图2所示,
随pH的变化如图2所示,![]() 下列有关LiH2PO4溶液的叙述正确的是
下列有关LiH2PO4溶液的叙述正确的是
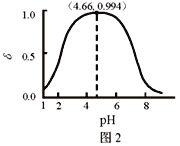
A. 含P元素的粒子有H2PO4–、HPO42–、PO43–
B. LiH2PO4溶液中存在2个平衡
C. 用浓度大于1 mol·L-1的H3PO4溶液溶解Li2CO3,当pH达到4.66时,H3PO4几乎全部转化为LiH2PO4
D. 随c初始(H2PO4–)增大,溶液的pH明显变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】众所周知H2S、SO2、NO和CO都是常见的大气污染物。
(1)下列关于H2S和SO2的说法正确的是______
A.两气体都可用浓硫酸干燥
B.两气体均可以用NaOH溶液吸收
C.可用溴水或酸性KMnO4溶液鉴别两气体
(2)目前治理汽车尾气是在催化剂条件下发生反应2NO+2CO![]() N2+2CO2,现在实验室模拟上述反应,已知t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
N2+2CO2,现在实验室模拟上述反应,已知t℃时在2L恒容密闭容器中加入2 molNO和1mol CO气体,经l0min达到平衡,测得此时CO2的体积分数为1/7,回答下列问题:
①这段时间内用CO表示的化学反应速率为_________________ 。
②该反应平衡常数为______________(保留两位有效数字)。
③平衡后再向密闭容器通入0.4molCO和0.4molCO2,平衡将_____________(填“正向”、“逆向”或“不”)移动。判断理由是_____________。
④若升温发现体系气体平均相对分子质量增大,则该反应的△H______0(填“>”、“<”或“=”)。
⑤维持条件不变,向平衡后的容器再充入0.2molNO和0.1molCO,达到新平衡,则与原平衡相比NO的转化率____________ (填“增大”、“减小”或“不变”)。
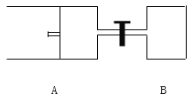
(3)如图所示,向A中充入 1mol X和1mol Y,向B中充入 2mol X和2mol Y,起始时VA=VB=aL。在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:X+Y![]() 2Z+W;(四物质均为气体)。达到平衡时VA=1.2a L,试回答:
2Z+W;(四物质均为气体)。达到平衡时VA=1.2a L,试回答:
①A中X的转化率αA=______________
②A、B中X的转化率αA______αB(填“>、=、<”)。
③打开阀门,一段时间后又达到平衡时,A的体积为___ L(连通管中的气体体积不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,发生反应A(g)+B(g)![]() C(g) ΔH<0,达到平衡后根据下列图象判断:
C(g) ΔH<0,达到平衡后根据下列图象判断:
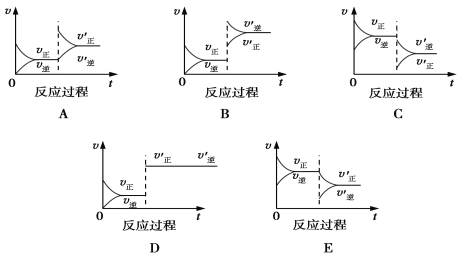
(1)表示升高温度,达到新平衡的是________(填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数________(填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是________,A的转化率________。
(3)表示减少C的量,达到新平衡的是______________。
(4)表示增加A的量,达到新平衡的是___________,此时B的转化率__________,A的转化率___________。
(5)表示使用催化剂,达到新平衡的是________________,C的质量分数________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com