
| A. | ①②③ | B. | ②③④⑤ | C. | ①③④⑤ | D. | ⑤⑥⑦ |
分析 原电池的形成条件:
1、有两种活泼性不同的金属(或其中一种为非金属导体)作电极;
3、电极均插入电解质溶液中;
3、两极相互连接(或接触);
4、能自发的发生氧化还原反应.
解答 解:A、①番茄②碳棒③导线,不存在两种活泼性不同的金属(或其中一种为非金属导体)作电极条件,不能形成原电池,故A错误;
B、②碳棒③导线④镁棒⑤铜棒,没有电解质溶液,不能形成原电池,故B错误;
C、①番茄③导线④镁棒⑤铜棒,番茄具有酸性能够与镁反应,符合原电池的构成条件,故C正确;
D、⑤铜棒⑥稀硫酸⑦烧杯,不存在两种活泼性不同的金属(或其中一种为非金属导体)作电极条件,不能形成原电池,故D错误;
故选C.
点评 本题考查了原电池的形成条件,难度不大,学生应学会根据原电池的形成条件来解答即可.


科目:高中化学 来源: 题型:解答题
| 键长/(pm) | B-F | B-Cl | B-Br |
| 计算值 | 152 | 187 | 199 |
| 实测值 | 130 | 175 | 187 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 试管中加入少量苯,加入溴水振荡后,溴水褪色,发生了加成反应 | |
| B. | 苯能使酸性高锰酸钾溶液褪色 | |
| C. | 苯较难发生加成反应,所以通常要加入催化剂 | |
| D. | 苯不能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
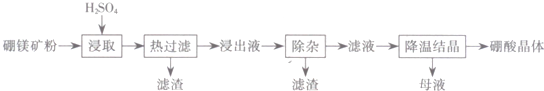
| 温度℃) | 20 | 40 | 60 | 100 |
| 溶解度(g) | 5.0 | 8.7 | 14.8 | 40.2 |
| 物质 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 3.2 | 5.2 | 9.7 | 12.4 |
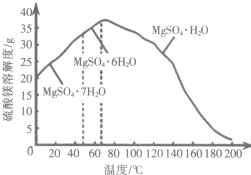
| 化学式 | H2CO3 | CH3COOH |
| 电离常数 | K1=4.4×10-7 K2=4.7×10-11 | K=1.75×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
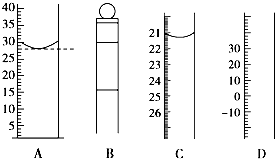 (1)图为常见仪器的部分结构(有的仪器被放大)
(1)图为常见仪器的部分结构(有的仪器被放大)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
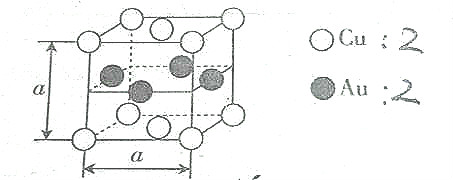
| A. | 该合金属于离子晶体 | B. | 该合金中Au的配位数是4 | ||
| C. | 该合金中Cu的配位数是8, | D. | 该合金的硬度低于Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com