

 +CH3OH→
+CH3OH→ +HCl.
+HCl. .
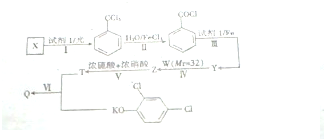
. 分析 根据题中各物质转化关系,由X→ 是在光照的条件下进行,符合烷烃取代反应的条件,从而推出X的结构简式
是在光照的条件下进行,符合烷烃取代反应的条件,从而推出X的结构简式 ;由Q:
;由Q: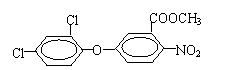 是由
是由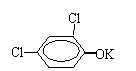 与T反应生成的,推出T的结构简式
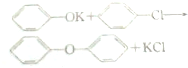
与T反应生成的,推出T的结构简式 ,Z在浓硫酸和浓硝酸作用下发生硝化反应生成T,则Z为
,Z在浓硫酸和浓硝酸作用下发生硝化反应生成T,则Z为 ,Y与相对分子质量为32的W发生信息①的反应生成Z,结合Z的结构可知,Y为
,Y与相对分子质量为32的W发生信息①的反应生成Z,结合Z的结构可知,Y为 ,W为CH3OH,据此答题;
,W为CH3OH,据此答题;
解答 解:根据题中各物质转化关系,由X→ 是在光照的条件下进行,符合烷烃取代反应的条件,从而推出X的结构简式
是在光照的条件下进行,符合烷烃取代反应的条件,从而推出X的结构简式 ;由Q:
;由Q: 是由
是由 与T反应生成的,推出T的结构简式
与T反应生成的,推出T的结构简式 ,Z在浓硫酸和浓硝酸作用下发生硝化反应生成T,则Z为
,Z在浓硫酸和浓硝酸作用下发生硝化反应生成T,则Z为 ,Y与相对分子质量为32的W发生信息①的反应生成Z,结合Z的结构可知,Y为
,Y与相对分子质量为32的W发生信息①的反应生成Z,结合Z的结构可知,Y为 ,W为CH3OH,
,W为CH3OH,
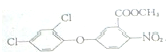
(1)根据Q的结构简式可知,Q的分子式为C14H9NO5Cl2,
故答案为:C14H9NO5Cl2;
(2)根据Q的结构简式可知,Q所含官能团有硝基、醚键和酯基、氯原子,
故答案为:酯基、氯原子;
(3)X的结构简式 ,X的名称是甲苯,反应Ⅲ是苯环上的氢原子被氯原子取代,所以反应类型是取代反应,
,X的名称是甲苯,反应Ⅲ是苯环上的氢原子被氯原子取代,所以反应类型是取代反应,
故答案为:甲苯;取代反应;
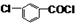
(4)反应Ⅳ的化学方程式为: +CH3OH→
+CH3OH→ +HCl,
+HCl,
故答案为: +CH3OH→
+CH3OH→ +HCl;
+HCl;
(5)根据上面的分析可知,T的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成、有机反应类型、化学方程式书写等,注意根据转化关系中有机物的结构进行推断,较好地考查学生自学能力、分析推理能力,难度中等


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | ⅠA族元素都是碱金属元素 | |
| B. | 碱金属单质可将铜从其盐溶液中置换出来 | |
| C. | 金属钾具有强还原性,K+具有强氧化性 | |
| D. | Cs常温下与水反应会发生爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
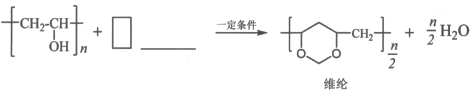
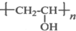 ,其工业合成路线如下:
,其工业合成路线如下: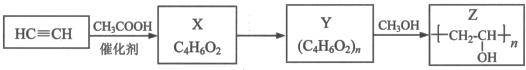
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Na2S溶液中:c(Na+)=c(HS-)+c(S2-) | |
| B. | 乙烯的燃烧热为akJ•mol-1(a>0),则乙烯燃烧的热化学方程式可表示为C2H4(g)+3O2(g)=2CO2(g)+2H2O(g)△H=-akJ•mol-1 | |
| C. | 钢铁发生吸氧腐蚀的正极反应式为O2+4e-+2H2O=4OH- | |
| D. | 从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
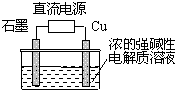 Cu2O是一种半导体材料,制取Cu2O的电解池如图,总反应为:2Cu+H2O$\frac{\underline{\;通电\;}}{\;}$Cu2O+H2↑.下列说法不正确的是( )
Cu2O是一种半导体材料,制取Cu2O的电解池如图,总反应为:2Cu+H2O$\frac{\underline{\;通电\;}}{\;}$Cu2O+H2↑.下列说法不正确的是( )| A. | 铜电极发生氧化反应 | |
| B. | 铜电极接直流电源的负极 | |
| C. | 石墨电极上产生氢气 | |
| D. | 每生成1molCu2O时,就有2mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
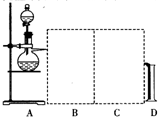
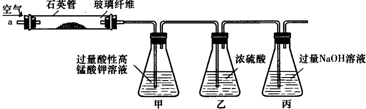
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 这两种烃一定是同分异构体 | |
| B. | 这两种烃不可能是同系物 | |
| C. | 在这两种烃的分子中,碳、氢原子个数之比一定相同 | |
| D. | 这两种烃各1mol完全燃烧,生成水的质量一定相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com