
| Ԫ�� | �����Ϣ |
| X | X�ǵؿ��к�������Ԫ�� |
| Y | YԪ��ԭ�Ӻ���3p�ܼ�����4������ |
| Z | ����Z��������Ϊ14��������Ϊ7 |
| T | T�ĵ�����һ�ֳ����Ľ����������Ƶ�������������Һ�����ڼ������ |
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٣��ڣ��ܣ��ۣ��� |
| B���ۣ��٣��ܣ��ڣ��� |
| C���ݣ��ۣ��ڣ��٣��� |
| D���ۣ��ܣ��ݣ��ڣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
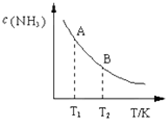 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺| һ������ |
| ʱ��/min Ũ��/mol?L-1 | c ��N2�� | c ��H2�� | c ��NH3�� |
| 0 | 0.6 | 1.8 | 0 |
| 3 | 0.52 | x | 0.16 |
| 6 | 0.36 | 1.08 | 0.48 |
| 9 | 0.36 | 1.08 | 0.48 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
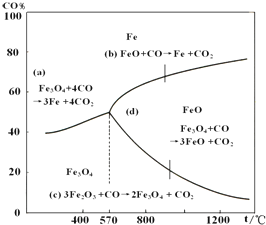 ������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯���������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ��������CO����������Ĺ�ϵ��ͼ��
������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯���������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ��������CO����������Ĺ�ϵ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
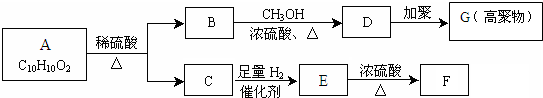
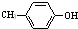 ��F��ʹ���CCl4��Һ��ɫ����ش��������⣺
��F��ʹ���CCl4��Һ��ɫ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
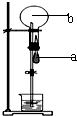 a��ʾ��ͷ�ι��е�Һ�壬b��ʾ��ƿ�е����壮�����γ���Ȫʵ�������a��Һ���b�����������ǣ�������
a��ʾ��ͷ�ι��е�Һ�壬b��ʾ��ƿ�е����壮�����γ���Ȫʵ�������a��Һ���b�����������ǣ�������| A��a-NaOH��Һ��b-HCl���� |
| B��a-NaOH��Һ��b-CO2���� |
| C��a-HCl��Һ��b-NH3���� |
| D��a-ˮ��b-CO2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
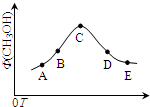 �������糧�ͷų��Ĵ��������NOx����SO2��CO2��Ի��������Ⱦ������Щ����������������̼�����������ɴﵽ���ܼ��š��������õ�Ŀ�ģ�
�������糧�ͷų��Ĵ��������NOx����SO2��CO2��Ի��������Ⱦ������Щ����������������̼�����������ɴﵽ���ܼ��š��������õ�Ŀ�ģ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ũ�Ⱦ�Ϊ0.02 mol?L-1��AgNO3��CH3COONa��Һ���һ������CH3COOAg���� |
| B����0.1 mol/LAgNO3��Һ��μ��뵽0.001mol/LKCl��0.001mol/LK2S��Һ�У��Ȳ���AgCl���� |
| C��ҪʹMg2+Ũ��Ϊ0.12 mol?L-1����Һ�в���Mg��OH��2�ij�������Һ��pH��9 |
| D����0.1mol/L AgNO3��Һ�еμ�0.1mol/LNaCl��Һ�������а�ɫ�������ɣ��������еμ�0.1mol/L��Na2S��Һ����ɫ����ת��Ϊ��ɫ�������������ӷ���ʽΪ��2Ag++S2-��aq��?Ag2S��s�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com