
| A. | △H4=$\frac{2}{3}$ (3△H3-△H1)-△H2 | B. | △H4=$\frac{2}{3}$ (△H1+△H2)+△H3 | ||
| C. | △H4=$\frac{2}{3}$ (△H1+△H2)-△H3 | D. | △H4=$\frac{2}{3}$ (△H1-△H2)-△H3 |
分析 H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H1①
2H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2 ②
2H2S(g)+O2(g)═2 S(g)+2H2O(g)△H3③,
将方程式$\frac{2}{3}$×①+$\frac{2}{3}$×②-③得2S(g)═S2(g),△H4进行相应的改变.
解答 解:H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H1①
2H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2 ②
2H2S(g)+O2(g)═2 S(g)+2H2O(g)△H3③,
根据目标方程,把方程③反写,把方程②乘以$\frac{2}{3}$;把方程①乘以$\frac{2}{3}$;然后三者相加;即-△H3+△H2×$\frac{2}{3}$+△H1×$\frac{2}{3}$=$\frac{2}{3}$(△H1+△H2)-△H3,
故选C.
点评 本题考查了盖斯定律的应用,要注意方程式计量数的变化,及△H的符号的变化,掌握基础是解题关键,题目难度不大,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe3+、K+、ClO- 都可在该物质的溶液中大量共存 | |
| B. | 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色 | |
| C. | 向0.1mol•L-1该物质的溶液中逐滴滴加0.1mol•L-1NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如上图所示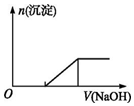 | |
| D. | 向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42-完全沉淀的离子方程式为:Fe2++2SO42-+2Ba2++2OH-═2BaSO4↓+Fe(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFe溶于过量硝酸,电子转移数为2NA | |
| B. | 1mol O2和2mol SO2反应生成的SO3分子数为2NA | |
| C. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子数为0.3NA | |
| D. | H2O2分解产生1molO2,转移的电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | Si-Si | O=O | Si-O |
| 键能/kJ•mol-1 | a | b | c |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.400mol•L-1 | B. | 0.300mol•L-1 | C. | 0.200mol•L-1 | D. | 0.100mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com