
����Ŀ���Ȼ���ͭ(CuCl)�ǰ�ɫ��ĩ������ˮ�����������²��ȶ��������ɽ��� Cu ��Cu2+���㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о���ѧϰС�����ȷֽ� CuC122H2O �Ʊ� CuCl�����������̽��������˵����ȷ����( )

A. ;�� 1 �в�����Cl2 ���Ի���ѭ�����ã�Ҳ����ͨ�뱥��CaCl2 ��Һ�г�ȥ
B. ;�� 2 �� 200��ʱ��Ӧ�Ļ�ѧ����ʽΪ��Cu2(OH)2Cl2![]() 2CuO+2HCl��
2CuO+2HCl��
C. X ���������N2��Ŀ������������������ CuCl22H2O ���ȹ��̿��ܵ�ˮ��
D. CuCl ��ϡ���ᷴӦ�����ӷ���ʽΪ��2CuCl��4H+��SO42��=2Cu2+��2Cl����SO2����2H2O
���𰸡�B
��������
Cl2�ڱ���CaCl2��Һ���ܽ�Ⱥ�С�����ܱ����գ�Cu2(OH)2Cl2���ȵ�200������CuO�����ԭ���غ���д����ʽ��X��������������CuCl2ˮ�⣻CuCl���������²��ȶ��������ɽ��� Cu ��Cu2+��
;��1�в�����Cl2����ת��ΪHCl������ѭ�����ã�Cl2�ڱ���CaCl2��Һ���ܽ�Ⱥ�С�����ܱ����ճ�ȥ����A����Cu2(OH)2Cl2���ȵ�200������CuO����ԭ���غ��֪��������HCl����ѧ����ʽΪ��Cu2(OH)2Cl2![]() 2CuO+2HCl����B��ȷ��CuCl2ˮ������������ͭ��HCl��X��������������CuCl2ˮ�⣬��XΪHCl�����ǵ�������C����CuCl���������²��ȶ��������ɽ��� Cu ��Cu2+����D����
2CuO+2HCl����B��ȷ��CuCl2ˮ������������ͭ��HCl��X��������������CuCl2ˮ�⣬��XΪHCl�����ǵ�������C����CuCl���������²��ȶ��������ɽ��� Cu ��Cu2+����D����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ����, ��Ա��еĢ١�����Ԫ�أ���д���пհף�
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� |
(1)�ߵ����ӽṹʾ��ͼ��__________��
(2)��������õĽ�����________(��дԪ�ط���)�����γɵ����ȶ���̬�⻯��Ļ�ѧʽ��_______��
(3)
(4)�ݡ����γɻ������к��еĻ�ѧ����________(�������Ӽ����������ۼ���)��
(5)1mol�ܵĵ����������ڵ��⻯����ȫ��Ӧ�����������ڱ�״���µ����Ϊ_____��
(6)д���ĵ�����ܵ�����������ˮ������Һ��Ӧ�Ļ�ѧ����ʽ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ���(ICl3)��ҩ��ϳ�����;�dz��㷺�����۵㣺33�棬�е㣺73�档ʵ���ҿ�����ͼװ����ȡICl3��
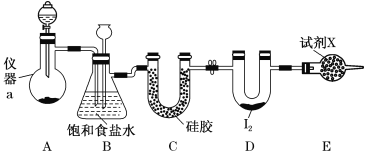
(1)����a��������________��
(2)�Ʊ�����ѡ�õ�ҩƷΪƯ������[��Ҫ�ɷ�ΪCa(ClO)2]��Ũ���ᣬ��ط�Ӧ�Ļ�ѧ����ʽΪ__________________________________��
(3)װ��B�����ڳ��ӣ�Ҳ�ǰ�ȫƿ���ܼ��ʵ�����ʱװ��C���Ƿ�����������д����������ʱװ��B�е�����____________________________________________��
(4)�Լ�XΪ________________��
(5)�����뵥�ʵ������¶��Ե���70���·�Ӧ����װ��D���˵ļ��ȷ�ʽΪ________________��
(6)500 mL(��״��)����CO��ij������Ʒͨ��ʢ������I2O5�ĸ���ܣ�170���³�ַ�Ӧ����ˮ���Ҵ����Һ����ܽ����I2�����ݵ�100 mL��ȡ25.00 mL��0.0100 mol��L��1 Na2S2O3����Һ�ζ������ı���Һ20.00 mL������Ʒ��CO���������Ϊ________��(������λ��Ч����)(��֪��������Ʒ�������ɷ���I2O5����Ӧ��2Na2S2O3��I2===2NaI��Na2S4O6)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���е���ɫ�仯����������ԭ��Ӧ�ص���
A | B | C | D | |
ʵ�� | NaOH��Һ����FeSO4��Һ�� | ʯ����Һ������ˮ�� | Na2S��Һ����AgCl��Һ�� | ��ͭ˿����ϡ������ |
���� | ������ɫ����������Ϊ���ɫ | ��Һ��죬���Ѹ����ɫ | �����ɰ�ɫ��Ϊ��ɫ | ������ɫ���壬����Ϊ����ɫ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Cl2��˵���У�����ȷ����
A. Cl2��һ�ֻ���ɫ���ж����� B. �����Cl2�ɱ����ڸ�ƿ��
C. ��˿��Cl2��ȼ������FeCl3 D. ������Һ�������ֲ�ͬ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ�ϵͳ���з�ӦC(s)��CO2(g) ![]() 2CO(g)����ʹ��Ӧ�����ӿ��Ĵ�ʩ��
2CO(g)����ʹ��Ӧ�����ӿ��Ĵ�ʩ��
��ͨ����С�����������ѹǿ�� �������¶� �۽�̿���顡 ��ͨ��CO2�� ������̿���� ����������ͨ��N2ʹ��ѹǿ����
A. �٢ڢۢ�B. �٢ڢܢ�C. �٢ڢۢ�D. �٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е�����ָ����Һ��һ���ܴ����������(����)
A. c(FeCl3)��1.0 mol��L��1����Һ�У�HCO![]() ��Cl����H����Na��
��Cl����H����Na��
B. �����£���ˮ�������c(H��)��10��14mol��L��1��Һ�У�NH![]() ��K����CO
��K����CO![]() ��SO
��SO![]()
C. ��c(HCO![]() )��0.1 mol��L��1����Һ�У�NH
)��0.1 mol��L��1����Һ�У�NH![]() ��AlO
��AlO![]() ��Cl����NO
��Cl����NO![]()
D. �����£� 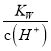 ��0.1 mol��L��1����Һ�У�K����NH3��H2O��SO
��0.1 mol��L��1����Һ�У�K����NH3��H2O��SO![]() ��NO
��NO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ���
A. NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)![]() NaOH(aq)
NaOH(aq)
B. Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
C. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
D. Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ�����ϡ����Ļ����Һ200mL��ƽ���ֳ����ȷݡ�������һ��������ͭ�ۣ�������ܽ�19.2g (��֪����ֻ����ԭΪNO����)������һ�����������ۣ�������������������������ӵı仯����ͼ��ʾ�����з��������������

A. OA�β�������NO��AB�εķ�ӦΪFe+2Fe3+=3Fe2+��BC�β�������
B. ԭ�������SO42�����ʵ���Ϊ0.6 mol
C. �ڶ�����Һ����������ΪFeSO4
D. ȡ20mLԭ������ˮϡ����1L����Һ��c(H+)=0.2mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com