
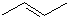 某有机物X的键线式为
某有机物X的键线式为 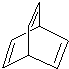
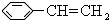 ,该芳香烃Z在一定条件下可发生聚合反应,写出其反应的化学方程
,该芳香烃Z在一定条件下可发生聚合反应,写出其反应的化学方程 .
.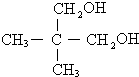 .
. 分析 (1)烃的键线式中交点、端点为碳原子,用H原子饱和C的四价结构,结合有机物键线式书写其分子式;
(2)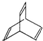 与足量的H2在一定条件下反应可生成环状的饱和烃为
与足量的H2在一定条件下反应可生成环状的饱和烃为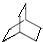 ,据此可判断它的一氯代物的同分异构体;
,据此可判断它的一氯代物的同分异构体;
(3)由有机物X的键线式为 可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键;
可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键;
(4)某醇W与X的相对分子质量相同,1mol W与足量Na反应能产生标准状况下的氢气22.4L,说明W中含有2个羟基,经测定W分子有如下特点:①一个碳原子最多连接一个官能团羟基;②该分子不存在官能团位置异构现象,W的结构简式为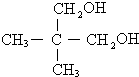 .
.
解答 解:(1)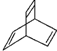 分子中含有8个碳原子和8个氢原子,其分子式为C8H8,故答案为:C8H8;
分子中含有8个碳原子和8个氢原子,其分子式为C8H8,故答案为:C8H8;
(2) 与足量的H2在一定条件下反应可生成环状的饱和烃为
与足量的H2在一定条件下反应可生成环状的饱和烃为 ,它的一氯代物有
,它的一氯代物有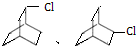 ,共2种,故答案为:2;
,共2种,故答案为:2;
(3)由有机物X的键线式为 可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,所以Y的结构简式为
可知,X的分子式为C8H8,其不饱和度为$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,所以Y的结构简式为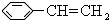 ,在一定条件下可发生聚合反应,方程式为
,在一定条件下可发生聚合反应,方程式为 ,
,
故答案为: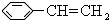 ;
;
(4)某醇W与X的相对分子质量相同,1mol W与足量Na反应能产生标准状况下的氢气22.4L,说明W中含有2个羟基,经测定W分子有如下特点:①一个碳原子最多连接一个官能团羟基;②该分子不存在官能团位置异构现象,W的结构简式为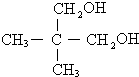 ,故答案为:
,故答案为: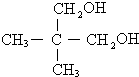 .
.
点评 本题考查有机物的推断,为高频考点,涉及同分异构体种类判断、有机物的性质、结构式的确定等知识点,侧重考查学生分析判断及计算能力,知道常见官能团发生的反应及其反应类型,题目难度不大.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 干冰熔化或升华时,CO2分子内的C=O键会被破坏 | |
| B. | 乙炔与氢气反应会变成乙烯,碳原子的杂化类型由sp变为sp2 | |
| C. | 物质的状态变化,只需克服分子间作用力 | |
| D. | 分子中不可能含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7 | B. | 5 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | σ键是轴对称的,π键是镜像对称的 | |
| B. | σ键是“头碰头”式重叠,π键是“肩并肩”式重叠 | |
| C. | σ键不能断裂,π键容易断裂 | |
| D. | H原子只能形成σ键,O原子可以形成σ键和π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化吸热,故液氨常做制冷剂 | |
| B. | 为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气 | |
| C. | 浓硝酸和浓硫酸与铜反应都能表现出强氧化性和酸性 | |
| D. | 实验室可用氯化铵固体与氢氧化钠固体共热制氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
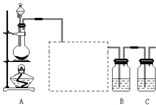 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11 | B. | 15 | C. | 22 | D. | 30 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com