
| A、豆科植物根瘤菌将含氮化合物转变为植物蛋白质 |
| B、植物从土壤中吸收含氮养料 |
| C、将空气中的氮气转变为含氮化合物 |
| D、将氨转变成硝酸及其它氮的化合物 |
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
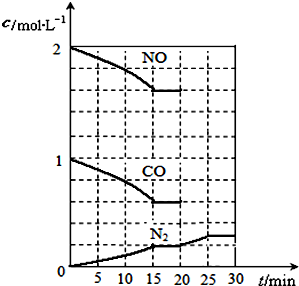 二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染.
二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molNaOH的摩尔质量为40g |
| B、NH4HCO3的相对分子质量为79g |
| C、64gSO2中含有1molO2 |
| D、0.5molCO2约含有3.01×1023个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是“康师傅”牌饮用矿泉水标签的部分内容(1mg=10-3g),从中可以推测( )
如图是“康师傅”牌饮用矿泉水标签的部分内容(1mg=10-3g),从中可以推测( )| A、该矿泉水中Mg2+的物质的量浓度的最大值为2×10-4 mol?L-1 |
| B、该矿泉水中Mg2+的物质的量浓度的最大值为1×10-4 mol?L-1 |
| C、1瓶该纯净水中SO42-物质的量的最大值为1×10-3mol |
| D、1瓶该纯净水中Cl-物质的量的最大值为1×10-3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2难溶于水,其水溶液的导电性极弱 |
| B、CaCl2的熔、沸点较高,硬度较大 |
| C、CaCl2固体不导电,但在熔融状态下可以导电 |
| D、CaCl2在有机溶剂(如苯)中的溶解度极小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4L |
| B、500mL1.0 mol?L-1NaNO2溶液含有溶质质量为34.5g |
| C、等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比小于3:1 |
| D、1.00molNaCl中含有6.02×1023个NaCl分子,欲配制1.00L,1.00mol.L-1的NaCl溶液,可将 58.5gNaCl溶于 1.00L水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com