
| X | Y | ||
| Z | W | ||
| T |
| A. | 根据元素周期律,可以推测存在T3Y4、TZ2和TW4 | |
| B. | X氢化物的沸点一定比Y氢化物的沸点低 | |
| C. | XZ2、XW4与YW3都是非极性分子 | |
| D. | W的氧化物的水化物酸性一定比Z的强 |
分析 X、Y、Z、W为短周期元素,T为第四周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故X为碳元素,X、T同主族,则T为Ge元素;Y与X同周期相邻,则Y为N元素;由元素在周期表中的位置可知,Z为S元素,W为Cl,然后结合元素周期律及元素化合物知识来解答.
解答 解:X、Y、Z、W为短周期元素,T为第四周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故X为碳元素,X、T同主族,则T为Ge元素;Y与X同周期相邻,则Y为N元素;由元素在周期表中的位置可知,Z为S元素,W为Cl,
A.Ge的化合价为+2和+4价,可以推测存在Ge3N4、GeS2和GeCl4,故A正确;
B.Y氢化物含氢键沸点较高,但X的氢化物不确定,可能常温下为固体,则X氢化物的沸点不一定比Y氢化物的沸点低,故B错误;
C.CS2、CCl4都是非极性分子,NCl3为极性分子,为三角锥型,故C错误;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性W(Cl)>Z(S),所以W的最高价氧化物对应水化物的酸性比Z的强,不是最高价无此规律,故D错误;
故选A.
点评 本题考查位置、结构、性质的关系,为高频考点,把握元素的位置、原子结构推断元素为解答的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Mg2+、Cl-、NO3-能大量共存于pH=0的溶液中 | |
| B. | 1 L浓度为l mol•L-1的NH4Cl溶液中含有NA个NH4+ | |
| C. | 除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO | |
| D. | 反应MnO2+ZnS+2H2SO4═MnSO4+ZnSO4+S+2H2O中,每析出12.8 g S共转移0.8mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| B. | 葡萄糖可用于补钙药物的合成 | |
| C. | 天然药物无任何毒副作用,可长期服用 | |
| D. | 超导陶瓷、高温结构陶瓷和光导纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用规格为100mL的量筒量取89.7mL蒸馏水 | |
| B. | 用容量瓶配制一定物质的量浓度的溶液前需用标准液润洗 | |
| C. | 打开分液漏斗、长颈漏斗、滴液漏斗的活塞,均可放出其中液体 | |
| D. | 锥形瓶、烧杯、烧瓶均可垫加石棉网加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质的电离方程式为KHXOn═K++H++XOn2- | |
| B. | 该溶液中水的电离程度比纯水的小 | |
| C. | 该溶液能与NaOH溶液发生中和反应 | |
| D. | 若该溶液显酸性,则K1•K2>10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
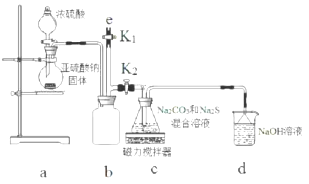
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 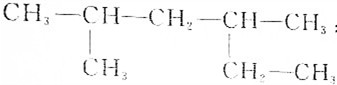 :2,4-二甲基已烷 :2,4-二甲基已烷 | |
| B. | 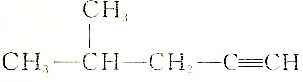 :2-甲基-4-戊炔 :2-甲基-4-戊炔 | |
| C. | 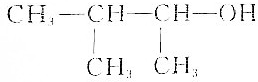 :3-甲基-2-丁醇 :3-甲基-2-丁醇 | |
| D. | CH2-CHBr-CHBr-CH3:2,3-二溴丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| B. | Fe2+(Fe3+),还原铁粉,过滤 | |
| C. | Cl2(HCl),饱和食盐水,洗气 | |
| D. | CO2(SO2),饱和NaHCO3溶液、浓硫酸,洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
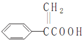 .下列有关说法中错误的是( )
.下列有关说法中错误的是( )| A. | 溴单质能与阿托酸发生加成反应 | |
| B. | 阿托酸能与硝酸发生取代反应 | |
| C. | 可用酸性KMnO4溶液区别阿托酸与苯 | |
| D. | 阿托酸分子中含有4个碳双键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com