
 是很强的氧化剂,在酸性溶液中它可将
是很强的氧化剂,在酸性溶液中它可将 氧化成
氧化成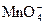 。取1支试管,加入少量
。取1支试管,加入少量 固体和2mL6 mol
固体和2mL6 mol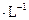
 ,然后滴入2mL1 mol
,然后滴入2mL1 mol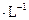
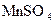 溶液。试回答:
溶液。试回答: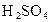 _______ _(填“能”或“不能”),用化学方程式回答
_______ _(填“能”或“不能”),用化学方程式回答 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 HSCN+HSCNO],它们阴离子的还原性强弱为:Cl-<Br-<SCN-<I-。试写出以下反应方程式:
HSCN+HSCNO],它们阴离子的还原性强弱为:Cl-<Br-<SCN-<I-。试写出以下反应方程式:查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.6mol | B.8mol | C.10mol | D.12mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3+2HCl=2NaCl+CO2↑+H2O | B.CaO+H2O=Ca(OH)2 |
C.2CO+O2 | D.CaCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com