
| A.2s轨道可以和3p轨道形成sp2杂化轨道 |
| B.烯烃中的碳碳双键由l个σ键和l个π键组成 |
| C.由极性键组成的分子,一定是极性分子 |
| D.甲烷中心原子sp3杂化轨道有一个由孤电子对占据 |
科目:高中化学 来源:不详 题型:单选题
电离能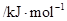 | 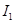 | 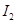 | 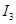 | 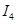 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲和乙所形成的化合物都是大气污染物 |
| B.原子半径:丙>乙>甲>丁 |
| C.气态氢化物的熔点:甲<丙 |
| D.最高价氧化物的对应水化物的酸性:丁>甲 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
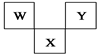
| A.三种元素的原子半径的大小顺序是W<Y<X |
| B.W最高价氧化物对应水化物具有强碱性,气态氢化物的水溶液具有弱酸性 |
| C.X元素的氧化物、氢化物的水溶液都呈酸性 |
| D.Y是周期表中非金属性最强的元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 (2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为_________________,该化学键能够形成的原因是 。
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为_________________,该化学键能够形成的原因是 。CH4 | SiH4 | NH3 | PH3 | |
沸点(K) | 101.7[ | 161.2 | 239.7  | 185.4 |
分解温度(K) | 873 | 773 | 1073  | 713.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HClO4 H2SO4 H3PO4 HSiO4 |
| B.HClO4 HClO3 HClO2 HClO |
| C.H2SO4 H2SO3 HNO3 HNO2 |
| D.HClO4H2SO4 H2SO3 H2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com