
【题目】对药物的认识和使用正确的是
A. 感冒时服用适量阿司匹林B. 大部分药物没有副作用
C. 创可贴能用于伤口消炎D. 胃酸过多只要冲服板蓝根冲剂即可治愈
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】提纯下列物质(括号内为少量杂质),所选用的除杂试剂与分离方法正确的是( )
不纯物质 | 除杂试剂 | 分离方法 | |
A | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 过滤 |
B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
C | 苯(Br2) | KOH溶液 | 分液 |
D | 苯(苯酚) | 浓溴水 | 过滤 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个体重50kg的健康人体内含铁元素2g,这2g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。请回答下列问题:
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是________________。
A .Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中__________是氧化剂,说明维生素C具有____性。
(3)己知下列反应: ①2I-+2Fe3+=2Fe2+ +I2 ②2Fe2++H2O2+2H+=2Fe3++2H2O, 则Fe3+ 、I2 、H2O2三者的氧化性由强到弱为____________________________。
(4)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中, HNO3表现的性质为_______ ,毎有1 molFe参加反应转移电子_____________mol。
(5)用双线桥标出该反应Fe+4HNO3=Fe(NO3)3+NO↑+2H2O电子转移的数目和方向______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合题。
(1)氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是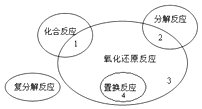
A.Cl2+2KBr═Br2+2KCl
B.2NaHCO3 ![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3
D.CH4+2O2CO2+2H2O
(2)高锰酸钾和氢溴酸溶液可以发生如下反应:
2KMnO4+16HBr═5Br2+2MnBr2+2KBr+8H2O
①其中还原剂 , 还原产物是 .
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为 , 转移电子的物质的量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸异戊酯是一种香料,其结构简式如图.下列有关肉桂酸异戊酯的叙述正确的是( ) 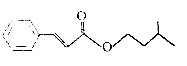
A.不能使溴的四氯化碳溶液褪色
B.能与新制的Cu(OH)2共热生成红色沉淀
C.能与FeCl3溶液反应显紫色
D.能与热的浓硝酸和浓硫酸混合液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥运场馆 “水立方” 顶部和外部使用了一种新型膜材料,它与制作塑料袋的材料类型相同,都属于
A. 光导纤维B. 有机合成材料C. 金属材料D. 玻璃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A、B、C、D、E、F、G在元素周期表中的位置如图1所示,回答下列问题: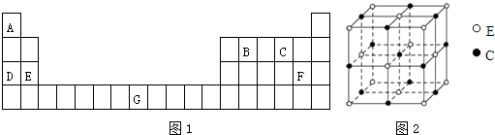
(1)G的基态原子核外电子排布式为 . 原子的第一电离能:DE(填“>”或“<”).
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l﹣l>l﹣b>b﹣b(l为孤对电子对,b为键合电子对),则关于A2C中的A﹣C﹣A键角可得出的结论是 .
A.180°
B.接近120°,但小于120°
C.接近120°,但大于120°
D.接近109°28′,但小于109°28′
(3)化合物G(BC)5的熔点为﹣20℃,沸点为103℃,其固体属于晶体,该物质中存在的化学键类型有 , 它在空气中燃烧生成红棕色氧化物,反应的化学方程式为 .
(4)化合物BCF2的立体构型为 , 其中B原子的杂化轨道类型是 , 写出两个与BCF2具有相同空间构型的含氧酸根离子 .
(5)化合物EC的晶胞结构如图2所示,晶胞参数a=0.424nm.每个晶胞中含有个E2+ , 列式计算EC晶体的密度 gcm﹣3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一定量的钠铝合金置于水中,合金全部溶解,所得的溶液中仍含有0.02mol的NaOH ,然后向溶液中逐滴加入lmol/L的盐酸,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )
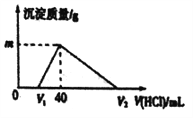
A. 原合金质量为0.92g B. 图中V2的值为60mL
C. 产生氢气的体积为1120mL D. 图中m的值为1.56g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com