
【题目】下列离子方程式书写正确的是( )
A.石灰乳与碳酸钠溶液反应:Ca2++CO32﹣=CaCO3↓
B.NH4HSO3溶液与足量的氢氧化钠溶液混合加热:NH4++HSO3﹣+2OH﹣ ![]() NH3↑+SO32﹣+2H2O
NH3↑+SO32﹣+2H2O
C.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3﹣+5I﹣+3H2O=3I2+6OH﹣
D.AgNO3溶液中加入过量的氨水:Ag++NH3?H2O=AgOH↓+NH4+
【答案】B
【解析】解:A.碳酸钠溶液与石灰乳的反应中,氢氧化钙不能拆开,正确的离子方程式为:CO32﹣+Ca(OH)2═CaCO3↓+2OH﹣ , 故A错误;
B.NH4HSO3溶液与足量的氢氧化钠溶液混合加热,反应生成氨气、亚硫酸钠和水,反应的离子方程式 为:NH4++HSO3﹣+2OH﹣ ![]() NH3↑+SO32﹣+2H2O,故B正确;
NH3↑+SO32﹣+2H2O,故B正确;
C.酸性条件下KIO3溶液与KI溶液发生反应生成I2 , 产物中不能存在氢氧根离子,正确的离子方程式为:6H++IO3﹣+5I﹣=3I2+3H2O,故C错误;
D.AgNO3溶液中加入过量的氨水,先发生反应:Ag++NH3H2O=AgOH↓+NH4+ , 氨水过量后后发生反应:AgOH+2NH3H2O=[Ag(NH3)2]++OH﹣+2H2O,不会生成沉淀,故D错误;
故选B.


科目:高中化学 来源: 题型:
【题目】2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,生成71g Cl2转移的电子是__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,向容积为2L的密闭容器中充入一定量的X气体和Y气体,发生如下反应:
X(g)+2Y(g) ![]() Z(g);反应过程中测定的部分数据见下表:
Z(g);反应过程中测定的部分数据见下表:
反应时间/min | n(X)/mol | n(Y)/ mol |
0 | 2.00 | 2.40 |
10 | 1.00 | |
30 | 0.40 |
下列说法正确的是( )
A.前10 min内反应的平均速率为v(Z)=0.10 mol·L-1·min-1
B.温度为200℃时,上述反应平衡常数为20,则正反应为吸热反应
C.若密闭容器体积可变,其他条件不变,在达到平衡后缩小容器体积为原来一半,则c(X)<1mol/L
D.保持其他条件不变,向容器中再充入1.00 mol X气体和1.20 mol Y气体,到达平衡后,X转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( ) 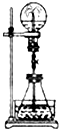
A.Cu与稀盐酸
B.NH4HCO3与稀盐酸
C.CaCO3与稀硫酸
D.NaHCO3与NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表的一部分,请参照元素①﹣⑧在图中的位置,用化学用语回答下列问题: 
(1)④、⑤、⑥的离子半径由大到小的顺序为 .
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 .
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: .
(4)由图中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,可使用的催化剂为(填序号) .
A.MnO2
B.KMnO4
C.Na2SO3
D.FeCl3
(5)②、③、④的气态氢化物的稳定性由强到弱的顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离的方程式,正确的是( )
A.CH3COOH═CH3COO﹣+H+?
B.NaOH═Na++OH﹣
C.H2SO4═H++SO ![]() ?
?
D.KClO3═K++Cl﹣+3O2﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com