
用H2O2溶液处理含NaCN的废水,反应原理为NaCN+H2O2+H2O=NaHCO3+NH3,已知:HCN的酸性比H2CO3弱。下列有关说法正确的是 ( )
A.该反应中氮元素被氧化
B.该反应中H2O2作还原剂
C.实验室配制NaCN溶液时,需加入适量的NaOH溶液
D.每生产0.1mol NaHCO3转移电子数约为0.1×6.02×1023个
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:2016-2017学年贵州铜仁市高二上期中考试化学试卷(解析版) 题型:选择题
一定温度下,可逆反应3X(g)+Y(g) 2Z(g)达到平衡的标志是:
2Z(g)达到平衡的标志是:
A.单位时间内生成3nmolX,同时生成nmolY
B.2v逆(Y)=v正(Z)
C.X、Y、Z的浓度相等
D.X、Y、Z的分子个数比为3:1:2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽铜陵市高一上期中考试化学试卷(解析版) 题型:选择题
某MgSO4和H2SO4的混合溶液中,c(Mg2+)=2mol/Lc(SO42-)=3mol/L,若将100mL此混合溶液中的Mg2+沉淀完全,最少需加2mol/L的 NaOH溶液体积是
NaOH溶液体积是
A.100mL
B.200mL
C.300mL
D.400mL
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、六合等七校高三上期中化学试卷(解析版) 题型:填空题
数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果。如利用CO2和CH4重整可制合成气(主要成分为CO、H2),已知重整过程中部分反应的热化学方程式为:
I、CH4(g)=C(s)+2H2(g) △H=+75.0kJ·mol-1
II、CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41.0kJ·mol-1
III、CO(g)+H2(g)=C(s)+H2O(g) △H=-131.0kJ·mol-1
(1)反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的△H = kJ·mol-1。
(2)固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。
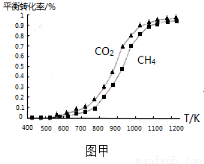

①同温度下CO2的平衡转化率 (填“大于”或“小于”)CH4的平衡转化率,其原因是 。
②高温下进行该反应时常会因反应I生成“积碳”(碳单质),造成催化剂中毒,高温下反应I能自发进行的原因是 。
(3)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图乙所示,该反应的化学方程式为 。
(4)CO常用于工业冶炼金属,右图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[c(CO)/c(CO2)]与温度(t)的关系曲线图。下列说法正确的是 。
A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D.CO还原PbO2的反应ΔH>0
(5)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极,KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,总反应的化学方程式为:2CO2 2CO+O2,则其阳极的电极反应式为 。
2CO+O2,则其阳极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、六合等七校高三上期中化学试卷(解析版) 题型:选择题
根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结 论 |
A | 测定等浓度的Na2CO3和Na2SO3 溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
B | 溴乙烷与NaOH溶液共热后,加入AgNO3溶液 | 未出现淡黄色沉淀 | 溴乙烷没有水解 |
C | 向等浓度的KCl、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层液体显紫红色 | 氧化性:Fe3+>I2 |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、六合等七校高三上期中化学试卷(解析版) 题型:选择题
下列有关物质的性质与用途具有对应关系的是 ( )
A.SO2具有还原性,可用于漂白纸浆
B.NH4HCO3受热易分解,可用作氮肥
C.氢氧化铝具有弱碱性,可用作净水剂
D.常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸
查看答案和解析>>
科目:高中化学 来源:2017届广东省韶关市六校高三上10月联考化学试卷(解析版) 题型:实验题
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

生成氢氧化物沉淀的pH:
Mg(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 9.4 | 6.3 | 1.5 |
完全沉淀时 | 12.4 | 8.3 | 2.8 |
(1)MgCO3 与稀硫酸反应的离子方程式为_______________________。
(2)加双氧水的目的______________________;相关的离子方程式_________________________;加氨水调节溶液的PH范围为______________。
(3)滤渣2 的成分是_____________(填化学式)。
(4)煅烧过程存在以下反应:2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体可以是________________(填化学式)。
②B中盛放的溶液可以是________________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北正定中学高一上第一次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加徳罗常数,下列叙述正确的是
A.标准状况下,22.4LH2O含有的分子数为NA
B.常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA
C.通常状况下,NA个CO2分子占有的体积为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源:贵州省铜仁市2016-2017学年高一上期中化学试卷(解析版) 题型:选择题
下列电解质溶于水时的电离方程式中,书写正确的是
A.H2SO3 2H++SO32-
2H++SO32-
B.NaHSO4=Na++H++SO42-
C.NaHCO3=Na++H++CO32-
D.K2SO4=K2++SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com