
【题目】实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称量的NaCl的质量分别是( )
A. 950mL,111.2g B. 500mL,117g
C. 1000mL,l17g D. 任意规格,117g
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 糖类化合物也可称为碳水化合物
B. 维生素D可促进人体对钙的吸收
C. 蛋白质是仅由碳、氢、氧元素组成的物质
D. 硒是人体必需的微量元素,但不宜摄入过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各溶液的叙述中正确的是( )
A. NaHSO3与Na2SO3混合溶液中一定存在如下关系:2c(Na+)=3(c(HSO3﹣)+c(SO32﹣)+c(H2SO3))
B. 向0.1molL﹣1的醋酸钠溶液中滴加0.1molL﹣1盐酸至中性,所得溶液中:c (Na+)>c (CH3COO﹣)>c (Cl﹣)=c (CH3COOH)>c(H+)=c(OH﹣)
C. 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣)
D. 向1.00 L 0.3molL﹣1NaOH溶液中缓慢通入0.2molCO2气体,溶液中:c(Na+)>c(CO32﹣)>c(HCO3﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是
A. pH=6.5的溶液一定显酸性
B. 0.1mol L-1的Na2CO3溶液中:c(CO32-)+c(HCO3-)=0.1mol L-1
C. 常温下,等体积的0.2 mol L-1的盐酸与0.2 mol L-1的氢氧化钡溶液混合,所得溶液的pH=13
D. 常温下,某溶液中水电离出的c(OH-)=l×10-12 mol L-1,该溶液pH 一定等于2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸合铁酸钾晶体Kx[Fe(C2O4)y]3H2O是一种光敏材料,下面是一种制备草酸合铁酸钾晶体的实验流程.
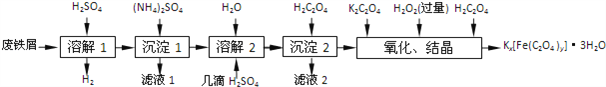
已知:(NH4)2SO4、FeSO47H2O、莫尔盐[(NH4)2SO4FeSO46H2O]的溶解度如下表:
温度/℃ | 10 | 20 | 30 | 40 | 50 |
(NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
FeSO47H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | ﹣ |
(NH4)2SO4FeSO46H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(1)“溶解1”应保证铁屑稍过量,其目的是______.“溶解2”加“几滴H2SO4”的作用是______.
(2)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、______、过滤、用乙醇洗涤、干燥.用乙醇洗涤的目的是______.
(3)“沉淀”时得到的FeC2O42H2O沉淀需用水洗涤干净.检验沉淀是否洗涤干净的方法是______.
(4)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是______.
(5)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤【备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液】:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250mL待测液.
步骤2:用移液管移取25.00mL待测液于锥形瓶中,加入稀H2SO4
步骤3:向步骤2所得溶液中______加热至充分反应(溶液黄色刚好消失),过滤、洗涤、将过滤及洗涤所得溶液收集到锥形瓶中.
步骤4:用c molL﹣1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是课外活动小组设计的用化学电源使LED灯发光装置.下列说法不正确的是( ) 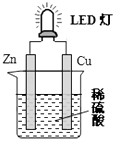
A.锌是负极,电子从锌片经导线流向铜片
B.氢离子在铜片表面被还原
C.装置中存在“化学能→电能→光能”的转换
D.如果将硫酸换成橙汁,导线中不会有电子流动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的叙述,正确的是
A.淀粉、纤维素和油脂都属于天然高分子化合物
B.糖类、植物油和蚕丝在一定条件下都能够发生水解反应
C.石油的分馏所得的馏分一定都是纯净物
D.苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A: 4HCl+O2 ![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.
ⅱ. 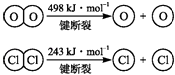
(1)反应A的热化学方程式是 .
(2)断开1mol H﹣O键与断开1mol H﹣Cl键所需能量相差约为kJ,H2O中H﹣O键比HCl中H﹣Cl键(填“强”或“弱”) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的.如图为一“链状连环”图案,图案上由左到右分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分由左到右A、B、C、D为其相应的分类依据代号.
请回答下列问题:
(1)请将分类依据代号填入相应的括号内.
两种物质都不是电解质
两种物质都是钠的化合物
两种物质都是氧化物
两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1molL﹣1的上图中一种化合物的水溶液,可制得一种红色胶体.
①反应的化学方程式为 .
②如何用较简单的方法判断胶体是否制备成功? .
③向该胶体中逐滴加入HI稀溶液,会出现一系列变化:
a.先出现红褐色沉淀,原因是 .
b.随后红褐色沉淀溶解,此反应的离子方程式是 . ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com