
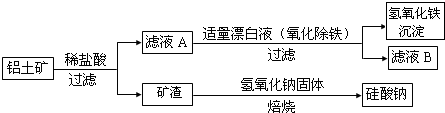
分析 图示工艺流程为:铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)加入稀盐酸,得到滤渣为二氧化硅,滤液中含有铁离子、亚铁离子和氯离子;加入漂白液后亚铁离子氧化成铁离子,铁离子水解生成氢氧化铁沉淀;滤液B为氯化铝溶液;二氧化硅与氢氧化钠在铁坩埚中焙烧生成硅酸钠,
(1)①检验是否含铁离子,可加入KSCN溶液;
②可先加入KSCN,在加入氯水;
③滤液B中铝元素为氯化铝,依据氢氧化铝溶液强酸强碱,不溶于弱碱选择;
(3)玻璃、瓷坩埚中含有二氧化硅,可与氢氧化钠在加热条件下反应.
解答 解:图示工艺流程为:铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)加入稀盐酸,得到滤渣为二氧化硅,滤液中含有铁离子、亚铁离子和氯离子;加入漂白液后亚铁离子氧化成铁离子,铁离子水解生成氢氧化铁沉淀;滤液B为氯化铝溶液;二氧化硅与氢氧化钠在铁坩埚中焙烧生成硅酸钠,
(1)①检验是否含铁离子,可加入KSCN溶液,如溶液变红色,可说明含有铁离子,故答案为:KSCN溶液或者硫氰化钾溶液;
②滤液B可能含有铁离子或亚铁离子,可取少量滤液B,加入KSCN溶液,若不变红,再加入少量氯水,仍然不变红,说明滤液B中不含铁元素,
故答案为:取少量滤液B,加入KSCN溶液,若不变红,再加入少量氯水,仍然不变红,说明滤液B中不含铁元素;
③滤液中含有的是氯化铝溶液,将滤液B中的铝元素以沉淀形式析出,
a.氢氧化钠溶液可以沉淀铝离子但过了会溶解氢氧化铝,氢氧化钠不是最佳试剂,故a错误;
b.硫酸溶液不与铝离子反应,故b错误;
c.二氧化碳和氯化铝不反应,无法生成氢氧化铝沉淀,故c错误;
d.氨水是弱碱不能溶解氢氧化铝,过量的氨水和铝离子形成氢氧化铝沉淀过滤得到氢氧化铝固体,故d正确;
故答案为:d;
(2)二氧化硅与盐酸不反应,矿渣中一定含有的物质是SiO2,
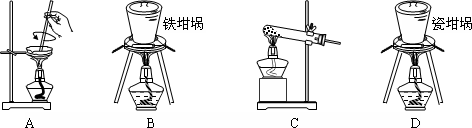
A.蒸发皿中含有二氧化硅和氢氧化钠反应,不能用于SiO2和NaOH焙烧制备硅酸钠,故A错误;
B.铁坩埚可以熔融二氧化硅和氢氧化钠,可在铁坩埚中用SiO2和NaOH焙烧制备硅酸钠,故B正确;
C.玻璃中含二氧化硅和氢氧化钠反应,不能用于SiO2和NaOH焙烧制备硅酸钠,故C错误;
D.瓷坩埚含有二氧化硅和氢氧化钠反应,不能用于SiO2和NaOH焙烧制备硅酸钠,故D错误;
故答案为:SiO2;B.
点评 本题考查了物质制备方案的设计、常见物质的分离与提纯方法的综合应用,题目难度中等,明确制备工艺流程及反应原理为解答关键,注意掌握化学实验基本操作方法,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5 9 6 | B. | 5 6 6 | C. | 3 9 7 | D. | 4 6 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | t0 | t1 | t2 | t3 | t4 | t5 |
| Φ(NO2) | $\frac{1}{3}$ | 0.30 | $\frac{4}{15}$ | $\frac{1}{6}$ | $\frac{1}{15}$ | $\frac{1}{15}$ |
| Φ(SO2) | $\frac{2}{3}$ | $\frac{19}{30}$ | 0.60 | 0.50 | 0.40 | 0.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡需加热的反应一定是吸热反应 | |
| B. | 相同条件下,2molH2(g)与lmolO2(g)完全化合生成2molH2O(g),放出aKJ热量,2molH2 (g)与lmolO2(g)完全化合生成2molH2O(l),放出bkJ 热量,则a>b | |
| C. | 若CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 | |
| D. | 相同条件下,1molH2O(l)与1molCaO完全化合,放出a kJ热量,2molH2O(l)与2molCaO完全化合,也放出a kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com