
[化学---选修5:有机化学基础]
偏四氯乙烷是一种常见化工原料,以偏四氯乙烷和烯烃(C5H10)为原料合成某种六元环酯(C7H10O4)的合成路线如下:已知:一个碳原子上连接2个—OH不稳定,容易脱水变成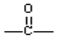

(1)化合物II中能与能与金属钠反应的官能团名称为_________________
(2)化合物IV合成化合物V的反应类型为______________化合物V合成化合物VI反应类型为_________________
(3)写出由化合物VI合成化合物VII的反应方程式________________________。
(4)有机物R是化合物IV的同分异构体,R能使溴水褪色,且其核磁共振氢谱中有4组峰,有机物R的结构简式为_________________,该六元环酯(C7H10O4)的结构简式为_________________
(5)参照上合成路线,设计以有机物( )和乙二醇为原料合成聚乙二酸乙二醇酯的合成路线。____________________________。
)和乙二醇为原料合成聚乙二酸乙二醇酯的合成路线。____________________________。
 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:计算题
100 mL H2、C2H6和CO2的混合气体与300 mL O2混合点燃,经充分反应并干燥后,总体积减少100 mL。再将剩余气体通过碱石灰吸收,体积又减少100 mL。上述体积均在同温同压下测定。求原混合气体中各组分的体积。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第三次质检化学试卷(解析版) 题型:选择题
在固定容积的密闭容器中,A和B发生下列反应,A(s)+2B(g) 2C(g)△H>0.在一定条件下达到平衡,若升高温度则达平衡后混合气体的
2C(g)△H>0.在一定条件下达到平衡,若升高温度则达平衡后混合气体的
A.平均相对分子质量增大 B.平均相对分子质量减小 C.密度减小 D. 气体压强增大
查看答案和解析>>
科目:高中化学 来源:2017届山东省日照市高三上学期期中化学试卷(解析版) 题型:选择题
一定条件下,A 、B、C存在如图所示的转化关系,其中△H=△H1+△H2。则A、C可能是( )
、B、C存在如图所示的转化关系,其中△H=△H1+△H2。则A、C可能是( )

①Fe、FeCl3 ②C、CO2 ③N2、NO2 ④Na、Na2O2 ⑤S、SO3
A.②④ B.②⑤ C.①④ D.③⑤
查看答案和解析>>
科目:高中化学 来源:2017届山东省日照市高三上学期期中化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.6.0 g SiO2晶体中含有的分子数为0.1NA
B.3.2g S2和S4的混合物中所含硫原子数一定为0.2NA
C.标准状况下,22.4 L NO和11.2 L O2混合后气体的分子总数小于NA
D.在反应KClO3+6HCl=KCl+3C12↑+3H2O中,当得到标准状况下67.2 L Cl2时,反应中转移的电子数为6NA
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列实验操作及现象和后面结论对应正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将SO2通入酸性高锰酸钾溶液 | 高锰酸钾溶液紫色褪色 | SO2具有漂白性 |
B | 向某溶液中滴加KSCN溶液 | 溶液显红色 | 原溶液中有Fe3+无Fe2+ |
C | 将稀硫酸滴入碳酸钠溶液中产生的气体通入硅酸钠溶液 | 有白色沉淀生成 | 证明非金属性S>C>Si |
D | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第三次周考化学卷(解析版) 题型:推断题
【化学-选修5:有机化学基础】部分果蔬中含有下列成分,回答下列问题:
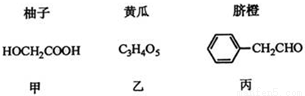
已知:
①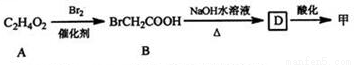
②1mol乙消耗NaHCO3的物质的量是甲的2倍
③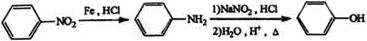
(1)甲可由已知①得到。
①甲中含有不饱和键的官能团名称为 ,可以表征有机化合物中存在任何官能团的仪器是 。
②A→B为取代反应,A的结构简式为 。
③B→D的化学方程式为 。
(2)乙在一定条件下生成链状脂类有机高分子化合物,该反应的化学方程式为 。
(3)由丙经下列途径可得一种重要的医药和香料中间体J(部分反应条件略去):
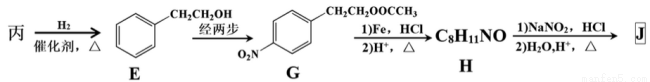
①检验丙中官能团的试剂是 ,反应的现象是 。
②经E→G→H保护的官能团是 ,据此推出E→G两步反应略去的反应物可能为:第一步 ,第二步 。
③J有多种同分异构体。其中某异构体L呈链状且不存在支链,L中的官能团都能与H2发生加成反应,L在核磁共振氢谱上显示为两组峰,峰面积比为3:2,则L的结构简式为 (只写一种)。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上11月月考化学卷(解析版) 题型:选择题
以H2、O2、熔融盐Na2 CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如下图所示,其中P端通入CO2。通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是
CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如下图所示,其中P端通入CO2。通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是
A.X、Y两端都必须用铁作电极
B.不可以用NaOH溶液作为电解液
C.阴极发生的反应是:2H2O+ 2e-= H2↑+ 2OH-
D.X端为电解池的阳极
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:实验题
金属及其化合物在生产中用途广泛。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶练铜的工艺流程如下:
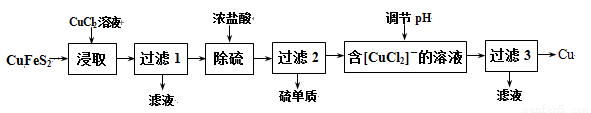
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有 ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为 。
Ⅱ.利用生产硼砂 的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
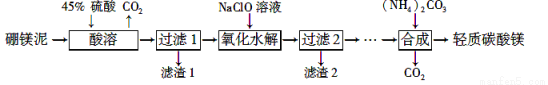
(1) 写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式 。
(2) 滤渣2的主要成分有MnO2和_____________,写出生成MnO2的离子方程式____________________。
(3)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是________________________(只需写出相应的化学方程式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com