
已知铅蓄电池放电时的电极反应:
负极:Pb+SO42-=PbSO4+2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
若用此电池(惰性电极)电解饱和食盐水,当阴、阳两极收集到的气体总体积为1.68L(标准状况)时,该蓄电池内消耗H2SO4______。
科目:高中化学 来源: 题型:
 我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列有关说法正确的是( )
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列有关说法正确的是( )| A、图中涉及的能量转化方式只有3种 | ||
B、蓄电池供电时,负极的电极反应为:Pb+SO
| ||
| C、储能时若充电时间过长,阳极流向阴极的气体可能是H2 | ||
| D、该发电工艺不可实现零排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
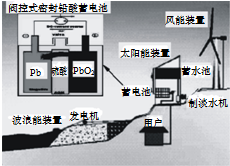
| A、图中涉及的能量转化方式只有3种 | B、蓄电池供电时,负极的电极反应为:Pb+SO42--2e-=PbSO4 | C、储能时若充电时间过长,阳极流向阴极的气体可能是H2 | D、该发电工艺可实现零排放 |
查看答案和解析>>
科目:高中化学 来源:2012届江苏省阜宁高中、大丰高中、栟茶高中高三第二次调研联考化学试卷 题型:单选题
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:
Pb+PbO2+2H2SO4 = 2PbSO4+2H2O,下列有关说法正确的是
| A.图中涉及的能量转化方式只有3种 |
| B.该发电工艺可实现零排放 |
| C.蓄电池供电时,负极的电极反应为:Pb-2e-=Pb2+ |
| D.储能时若充电时间过长,阳极流向阴极的气体可能是H2 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山西省临汾一中高一下学期期中考试化学试卷 题型:单选题
实验室用铅蓄电池作电源电解水,已知铅蓄电池放电时的电极反应如下:
负极:Pb + SO42――2e―="=" PbSO4
正极:PbO2 + 4H+ + SO42―+2e― ="=" PbSO4+ 2H2O
若制得0.1mol 的H2,此时电池内消耗的硫酸的物质的量至少是
| A.0.025 mol | B.0.50 mol | C.0.10 mol | D.0.20 mol |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省五校高三第一次联考化学试卷(解析版) 题型:选择题
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中,正确的是( )

A.由TiO2制得1mol 金属Ti ,理论上外电路转移2 mol电子
B.阳极的电极反应式为:C + 2O2- − 4e- == CO2↑
C.在制备金属钛前后,整套装置中CaO的总量减少
D.若用铅蓄电池作该装置的供电电源,“+”接线柱应连接Pb电极(已知铅蓄电池放电时的总反应为Pb + PbO2 + 2H2SO4 = 2PbSO4 + 2H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com