
| A. | 3:2 | B. | 2:3 | C. | 1:1 | D. | 5:4 |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量浓硫酸溅在皮肤上,立即用NaOH溶液冲洗 | |
| B. | 酒精洒在桌面上引起失火,可用水浇灭 | |
| C. | 轻度烧伤、烫伤可用冰水或者冷水降温止痛 | |
| D. | 误服可溶性钡盐,可及时服用Na2CO3溶液解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制取溴苯应用液溴、铁屑和苯混合,反应后先用水再用稀碱液洗涤 | |
| B. | 检验C2H5Cl中氯原子,将C2H5Cl和NaOH溶液混合加热后,加稀硫酸进行酸化 | |
| C. | 用无水乙醇和浓H2SO4共热至140℃可以制得乙烯气体 | |
| D. | 苯酚中滴加少量的稀溴水出现了三溴苯酚的白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
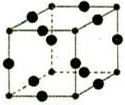 Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.
Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N×10-2 mol/L | B. | $\frac{N}{1.204×1022}$ mol/L | ||
| C. | $\frac{N}{6.02×1021}$mol/L | D. | $\frac{N}{6.02×1025}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1 | |
| B. | 由N2(g)+3H2(g)2NH3(g)△H=-92.4 kJ•mol-1热化学方程式可知,当反应中转移6NA(NA为阿伏加德罗常数的值)电子时,反应放出的热量等于92.4kJ | |
| C. | HCl和NaOH反应的中和热△H=-57.3kJ•mol-1,则H2SO4和KOH反应的中和热△H=-57.3kJ•mol-1 | |
| D. | 在101 kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=+571.6 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com