
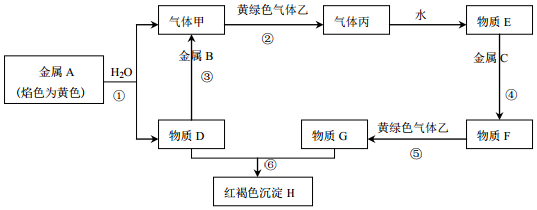
���� ����A�ǵؿ��к������Ľ�������AΪ����Al��Al�ڿ�����Ѹ�ٱ�����������������CΪAl2O3��H�������Σ���HΪAl��NO3��3��D��һ�ֵ���ɫ�Ļ������DΪNa2O2��E�ܹ����������Ӧ��������G����EΪNaOH��GΪH2��FΪNaAlO2��Al��NO3��3��NaAlO2���ܹ�ת����I����IΪAl��OH��3���ݴ˽��н��
��� �⣺����A�ǵؿ��к������Ľ�������AΪ����Al��Al�ڿ�����Ѹ�ٱ�����������������CΪAl2O3��H�������Σ���HΪAl��NO3��3��D��һ�ֵ���ɫ�Ļ������DΪNa2O2��E�ܹ����������Ӧ��������G����EΪNaOH��GΪH2��FΪNaAlO2��Al��NO3��3��NaAlO2���ܹ�ת����I����IΪAl��OH��3��
��1�����ݷ�����֪��DΪNa2O2��FΪ NaAlO2��IΪAl��OH��3��
�ʴ�Ϊ��Na2O2��NaAlO2��Al��OH��3��
��2������GΪ������Al������������Һ��Ӧ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ��2Al+2OH-+2H2O=2AlO2-+3H2����
H�백ˮ��Ӧ����I�����ӷ���ʽΪ��Al3++3NH3•H2O=Al��OH��3��+3NH4+��
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����Al3++3NH3•H2O=Al��OH��3��+3NH4+��
��3���������������۵�Զ��������������Ƭ�����ɵ�����������ס���ۻ�����ʹ�䲻���䣬
�ʴ�Ϊ�����������۵�Զ������������ס���ۻ�����ʹ�䲻���䣻
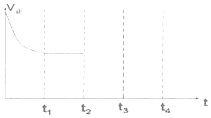
��4�������½�������Ũ���ᷢ���ۻ�������ֹ�˷�Ӧ�ļ������У������²���������Ũ������ȡ��������
�ʴ�Ϊ������������Ũ����ۻ���
���� ���⿼�����ƶϣ���Ŀ�Ѷ��еȣ���ȷ�ƶϸ���������Ϊ���ؼ���ע���������ճ���Ԫ�ؼ��仯�������ʣ�����������ѧ���ķ���������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ����Fe2+��Cu2+ | B�� | һ����Fe2+��Cu2+��������Fe3+ | ||
| C�� | һ����Fe2+��������Cu2+ | D�� | ֻ��Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ba2+��Cl-��SO42-��K+ | B�� | Mg2+��SO42-��Na+��Cl- | ||
| C�� | H+��CO32-��Al3+��Cl- | D�� | K+��S O32-��NO3-��H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 2016��12�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��
2016��12�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����ʵ | ���� |
| A | H2����Cl2��ȼ�� | ȼ�ղ�һ���������μ� |
| B | �����ھƾ��ƻ����ϼ����ۻ��������� | �������۵������ |
| C | �ƿ�Ͷ��ˮ�У�Ѹ���۳�����ɫС�� | �Ƶ��ܶȱ�ˮС |
| D | ij��Һ�м��������ữ��AgNO3��Һ��������ɫ���� | ����Һ�к���Cl- |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
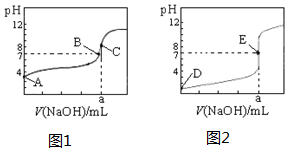 ��ͼΪ��������0.1000mol•L-1NaOH��Һ�ζ�20.00mL 0.1000mol•L-1�����20.00mL 0��.1000mol•L-1��������ߣ�����HA��ʾ�ᣬ�����жϺ�˵������ȷ���ǣ�������
��ͼΪ��������0.1000mol•L-1NaOH��Һ�ζ�20.00mL 0.1000mol•L-1�����20.00mL 0��.1000mol•L-1��������ߣ�����HA��ʾ�ᣬ�����жϺ�˵������ȷ���ǣ�������| A�� | ͼ2�ǵζ���������� | |
| B�� | ͼ1�ζ�ʱӦ��ѡ���̪��ָʾ�� | |
| C�� | B��ʱ����Ӧ������Һ�����V��NaOH����V��HA�� | |
| D�� | ��0 mL��V��NaOH����20.00 mLʱ����Ӧ��Һ�и�����Ũ�ȴ�С˳��һ����Ϊc��A-����c��Na+����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ���������ζ | B�� | 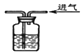 ��Ũ�������CO2 | ||
| C�� | 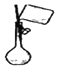 ������ƿ��ת��Һ�� | D�� | 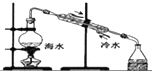 �ú�ˮ��ȡ��ˮ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com