
分析 (1)含有碳元素的化合物属于有机物;
(2)苯酚是一种有毒的物质,对人体有害;
(3)苯酚有毒,能够污染水体和土壤;应该挖隔离沟、铺薄膜防止扩散并回收泄漏的苯酚;要随时监测附近水源、土壤中的苯酚;
(4)苯酚燃烧生成二氧化碳和水.
解答 解:(1)苯酚的化学式为C6H6O,苯酚是含有碳元素的化合物,属于有机物;
故答案为:有机物;
(2)现场救护人员应佩戴呼吸器,穿好防化服的原因是苯酚有毒性,有强烈的腐蚀性;
故答案为:苯酚有毒性,有强烈的腐蚀性;
(3)用水进行冲洗或用泥土填埋能够污染水体和土壤;应该挖隔离沟、铺薄膜防止扩散并回收泄漏的苯酚;要随时监测附近水源、土壤中的苯酚;
故答案为:②③;
(4)苯酚燃烧生成二氧化碳和水,其反应的方程式为:C6H6O+7O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+3H2O;
故答案为:C6H6O+7O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+3H2O.
点评 本题考查了苯酚的性质和环境保护,题目难度不大,注意把握苯酚的化学性质,侧重于基础知识的考查.


科目:高中化学 来源: 题型:选择题
| A. | NaCl属于离子化合物 | B. | 原子团为OH-属于羟基 | ||
| C. | 乙醇与水混合后静置,不出现分层 | D. | 淀粉水解的最终产物含有葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
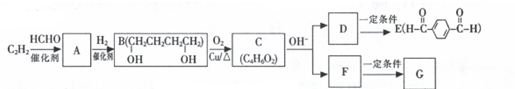

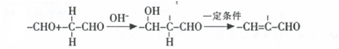
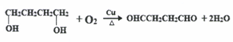 .
.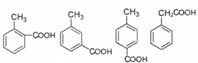 (任意一种)(任写一种).
(任意一种)(任写一种). $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$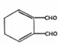 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
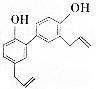 中药厚朴皮中起抗菌作用的有效成分为厚朴酚,其结构简式如图所示.该物质具有持久的肌肉松弛作用和极强的抗菌作用,临床上主要用于镇静中枢神经、抗真菌等.
中药厚朴皮中起抗菌作用的有效成分为厚朴酚,其结构简式如图所示.该物质具有持久的肌肉松弛作用和极强的抗菌作用,临床上主要用于镇静中枢神经、抗真菌等.| A. | 1个厚朴酚分子中含有16个碳原子 | |
| B. | 厚朴酚能使酸性KMnO4溶液褪色,遇FeCl3溶液显色 | |
| C. | 1mol厚朴酚与足量NaHCO3溶液反应放出22.4LCO2(标准状况) | |
| D. | 1mol厚朴酚能与4molBr2(Br2的CCl4溶液)反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属锗是一种良好的导热、导电材料 | |
| B. | 元素的非金属性越强,其氢化物的沸点越高 | |
| C. | 同周期相邻主族元素的原子,其质子数之差均为1 | |
| D. | 最外层电子数为4的原子,其元素一定处于ⅣA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
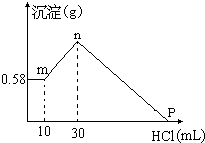
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
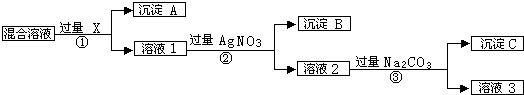
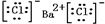 ,沉淀A的晶体类型离子晶体,CO32-的空间构型是平面三角形.
,沉淀A的晶体类型离子晶体,CO32-的空间构型是平面三角形.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com