
【题目】利用固体表面催化工艺进行NO分解的过程如下图所示。下列说法不正确的是

A.该分解过程是:2NO![]() N2+O2
N2+O2
B.实验室制取NO可以用铜与稀硝酸反应
C.过程②释放能量,过程③吸收能量
D.标准状况下,NO分解生成5.6 LN2转移电子数约为6.02×1023
【答案】C
【解析】
A.根据图示,NO在催化剂作用下转化为氮气和氧气,该分解过程是:2NO![]() N2+O2,故A正确;
N2+O2,故A正确;
B.铜与稀硝酸反应生成一氧化氮、硝酸铜和水,可以用于实验室制取NO,故B正确;
C.过程②为NO在催化剂表面发生断键形成氮原子和氧原子,断开化学键需要吸收能量,过程③为氮原子和氧原子重新形成化学键生成氮气和氧气,形成化学键需要释放能量,故C错误;
D.根据反应2NO![]() N2+O2,O元素由-2价变为0价,生成1mol O2,同时生成1molN2,转移4mol电子,标准状况下,NO分解生成5.6 LN2为0.25mol,则转移电子数约为0.25mol ×4×6.02×1023=6.02×1023个,故D正确;
N2+O2,O元素由-2价变为0价,生成1mol O2,同时生成1molN2,转移4mol电子,标准状况下,NO分解生成5.6 LN2为0.25mol,则转移电子数约为0.25mol ×4×6.02×1023=6.02×1023个,故D正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】煤的综合利用备受关注。有如下的转化关系,CO与H2不同比例可以分别合成A、B,已知烃A对氢气的相对密度是14,B能发生银镜反应,C为常见的酸味剂。

(1)有机物C中含有的官能团的名称是____________________。
(2)反应⑤的反应类型为______________。
(3)写出③的反应方程式 ____________。
(4)下列说法正确的是______________。(填字母)
A.第①步是煤的液化,为煤的综合利用的一种方法
B.有机物B和C都可以与新制氢氧化铜发生反应
C.有机物C和D的水溶液都具有杀菌消毒作用
D.乙酸乙酯与有机物D混合物的分离,可以用氢氧化钠溶液振荡、静置分液的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面物质间转换的框图,回答有关问题:
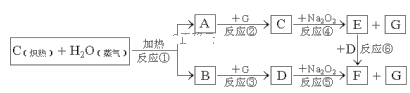
(1)写出框图中物质A和F指代物质的化学式:A___,F___;
(2)在反应①~⑥中属于非氧化还原反应的是___(填写序号);
(3)如果2molNa2O2与足量水蒸气反应生成O2,该反应中转移电子总数是___;
(4)如果A、B混合气体3.0g(平均摩尔质量15g·mol-1),在与G充分反应后,通过足量Na2O2,可使Na2O2增重___g,并得到O2___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用碱性溶液吸收多余的氯气,防止环境污染。某次实验中,将多余的氯气用100 mL 2.00 mol·L1的NaOH溶液恰好完全吸收,测得吸收液中ClO与ClO3的物质的量之比为5:1。
(1)吸收的氯气的物质的量为_____________。
(2)吸收液中Cl的物质的量浓度为______________(溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加。A是元素Y的单质。常温下,A遇甲的浓溶液发生钝化。丙、丁、戊是由这些元素组成的二元化合物,且丙是无色气体,上述物质的转化关系如下图所示,下列说法正确的是
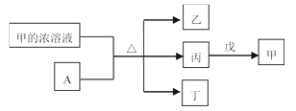
A.由于丁和戊化学键相同,所以它们都是平面结构
B.简单氢化物的沸点: X>Z
C.简单离子半径大小: X<Y
D.Y的简单离子与Z的简单离子在水溶液中可大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸盐在无机试剂制备中应用广泛。某研究小组用如下两种方法制备FeCO3。已知: FeCO3 是白色固体,难溶于水。
I.研究小组用炼铁厂的铁矾渣制备FeCO3,铁矾渣主要含有K2Fe6(SO4)4(OH)12、ZnO、Fe2O3及少量的CaO、MgO、 SiO2 等。
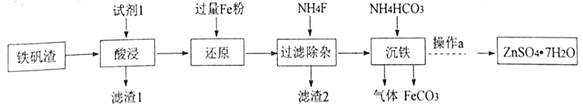
(1)试剂1是过量的_______,滤渣 2的成分是__________ (写化学式);
(2)“沉铁”发生反应的离子方程式是____________;
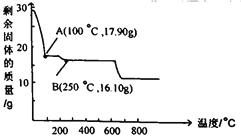
(3)沉铁后的滤液经“操作a”,再经过“过滤、 洗涤、干燥”得到皓矾(ZnSO4·7H2O),“操作a”是__,取28.70g皓矾(ZnSO4·7H2O)加热,剩余固体的质量变化如图,100°C时所得固体的化学式____。
II.研究小组又采用如下装置制取FeCO3 (C后及夹持装置略)。操作的关键是向Na2CO3溶液(pH=12.11)通入一段时间CO2至溶液pH为7,再滴加一定量FeSO4溶液,产生白色沉淀。
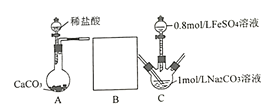
(1)画出装置B______________,B中所用试剂为______________;
(2)先向1mol/L Na2CO3溶液中通入CO2的目的是_________________________;
(3)FeCO3溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂,该实验小组用KMnO4测定补血剂中亚铁含量进而计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于100%,其原因是_______________(不考虑操作不当引起的误差)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是某抗炎症药物的中间体,其合成路线如下:
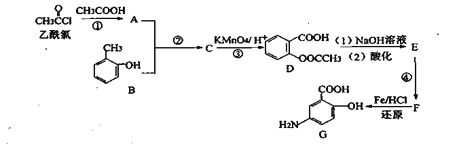
已知:①![]()
![]()
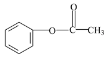
② ![]()
![]()
![]() (呈碱性,易氧化)
(呈碱性,易氧化)
(1)C的官能团名称是_______________;
(2)反应①的反应类型为___________;反应②的作用是___________________;
(3)下列对有机物G的性质推测不正确的是____________________ (填选项字母);
A.1molG与足量NaHCO3溶液反应放出2molCO2
B.能发生取代反应和氧化反应
C.能加聚合成高分子化合物
D.具有两性,既能与酸反应也能与碱反应
(4)写出E→F的化学反应方程式______________________________;
(5)同时符合下列条件的D的同分异构体有__________种:
①含有苯环且能发生水解反应:②能发生银镜反应;③能与NaHCO3溶液反应放出CO2。
(6)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位:苯环上有发基时,新引入的取代基连在苯环的问位。根据题中的信息,写出以甲苯为原料合成有机物的流程图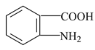 (无机试剂任选)_______________________________________________________________________________________。 合成路线流程图示例:X
(无机试剂任选)_______________________________________________________________________________________。 合成路线流程图示例:X![]() Y
Y![]() Z……目标产物
Z……目标产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取a mol某含氧衍生物的蒸气,使其与2a mol O2混合点燃,两者恰好完全反应,生成等体积的CO2和水蒸气,反应后混合气体的密度较反应前减少了![]() (均在相同条件下测定),则该有机物的分子式为 ( )
(均在相同条件下测定),则该有机物的分子式为 ( )
A.C2H4B.C3H6O2C.C2H4O2D.C4H8O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和活性炭的混合物用NaCl溶液浸润后,置于如图装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是( )
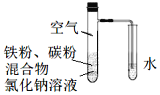
A.铁被氧化的电极反应式为Fe–3e=Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com