
根据下图所示装置和操作,回答下列有关问题。
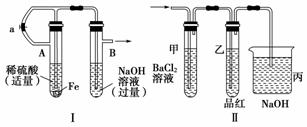
(1)按图Ⅰ所示装置,用两种不同的操作分别进行实验,观察B管中的现象。
①操作1:先夹紧止水夹a,再使A管开始反应,实验中观察到B管中的现象是_________________________________________________。
②操作2:打开止水夹a,使A管反应一段时间后再夹紧止水夹a,实验中观察到B管中的现象是________________________________________________。
③请说明造成两种操作现象不同的原因(如两种现象相同,此小题不用回答):_______________________________________________。
(2)上述装置实验结束后,取A管内反应所得的溶液,隔绝空气小心蒸干后,再高温煅烧(有关装置和操作均已略去),最后留下红色固体,将分解时产生的气体按图Ⅱ所示装置依次通过洗气装置,结果试管甲内出现白色沉淀,试管乙内品红溶液红色褪去,回答:
①用化学方程式表示试管甲产生白色沉淀的原因_________________________________________________。
②根据实验现象写出A管内溶液蒸干后,在高温煅烧分解时所发生的化学反应方程式__________________________________________________。
③图Ⅱ中丙装置的作用是_________________________________________________。
实验结束时,在装置丙中观察到的现象是_______________________________________________。
【解析】 当夹紧止水夹a使A试管进行反应时,产生的气体会将FeSO4压入B管内,与适量的NaOH反应生成白色Fe(OH)2沉淀,但由于系统中含有空气,生成的Fe(OH)2很快被氧化为Fe(OH)3,出现一系列的颜色变化。当先使A管反应一段时间后再打开止水夹,由于产生的H2将系统中的空气赶尽,使生成的Fe(OH)2不再被氧化。由于A管内H2SO4不过量,最后生成的溶质应为FeSO4,由信息知,FeSO4分解产物有SO3、SO2和Fe2O3。
【答案】 (1)①液面升高且生成白色沉淀,且迅速变为灰绿色,最后变为红褐色
②液面上升,有白色沉淀生成,且保持较长时间不变色
③产生的H2将系统内空气赶尽,避免了Fe(OH)2的氧化
(2)①SO3+H2O+BaCl2 BaSO4↓+2HCl
BaSO4↓+2HCl
②2FeSO4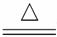 Fe2O3+SO3↑+SO2↑
Fe2O3+SO3↑+SO2↑
③吸收剩余的SO2气体 导管内倒吸一段液柱


科目:高中化学 来源: 题型:
有机化合物A~H的转换关系如下所示:
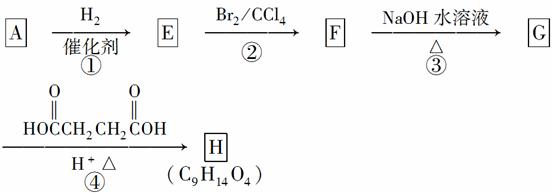
请回答下列问题:
(1)链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1mol A完全燃烧消耗7mol氧气,则A的结构简式是________,名称是________;
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E。由E转化为F的化学方程式是______________________________;
(3)G与金属钠反应能放出气体。由G转化为H的化学方程式是________;
(4)①的反应类型是______;③的反应类型是______;
(5)链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊烷,写出B所有可能的结构简式__________________________;
(6)C也是A的一种同分异构体,它的一氯代物只有一种
(不考虑立体异构),则C的结构简式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列物质的转化关系中,A是一种固体单质,且常作半导体材料,E是一种白色沉淀,F是最轻的气体单质。
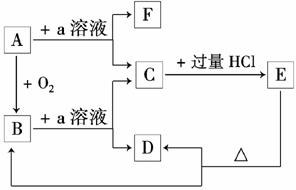
据此填写:
(1)B的化学式是________,目前在现代通讯方面B已被用作________的主要原料。
(2)B和a溶液反应的离子方程式是_________________________________
________________________________________________________________________。
(3)A和a溶液反应的离子方程式是_________________________________________
________________________________________________________________________。
(4)C和过量盐酸反应的离子方程式是__________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿佛加德罗常数的数值,下列说法正确的是
A.1L0.1mol•L-1 Na2CO3溶液中有NA个CO32-
B.常温常压下,22gCO2中共有2NA个共用电子对
C.0.1mol Na2O2与水完全反应,转移的电子数为0.2NA
D.2.8gN2、CO和C2H4组成的混合气体所占有的体积约为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氧化性Fe3+>I2。向Fe I 2溶液中通入一定量的Cl2,发生反应的离子方程式为:
a Fe2++b I-+c Cl2→d Fe3++ e I2+ f Cl- 。下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是
A.2,4,3,2,2,6 B. 0,2,1,0,1,2
C.2,0,1,2,0,2 D. 2,8,5,2,4,10
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用洗净的废铜屑作原料来制备硝酸铜。为了节约原料和防止污染环境,宜采取的方法是( )
A.Cu+HNO3(浓)―→Cu(NO3)2
B.Cu CuO
CuO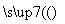 Cu(NO3)2
Cu(NO3)2
C.Cu+HNO3(稀)―→Cu(NO3)2
D.Cu CuSO4
CuSO4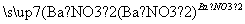 Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
法国里昂的科学家最近发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是( )
A.该粒子不显电性
B.该粒子质量数为4
C.在周期表中与氢元素占同一位置
D.该粒子质量比氢原子大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com