
| A、原反应物中CuO与Fe2O3物质的量的比为1:1. |
| B、反应后所得CO2的质量为40g |
| C、参加反应的CO的质量为11.2g |
| D、原反应物中CuO与Fe2O3物质的量的比为1:2. |
| 40g |
| 100g/mol |
| 40g |
| 100g/mol |
|


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、35.5a V2=w2-w1 | ||
| B、n(Na)=a V2 | ||
C、n(Na)+3n(Al)=
| ||
D、a V2=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.12g |
| B、6.42g |
| C、2.24g |
| D、3.24g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷 | B、丙烷 | C、丁烷 | D、戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
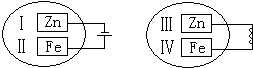 把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,观察到的现象和对应方程式都正确的是( )
把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,观察到的现象和对应方程式都正确的是( )| A、Ⅰ附近溶液变红,Zn-2e-=Zn2+ |
| B、Ⅳ附近溶液变红,O2+2H2O+4e-=4OH- |
| C、Ⅱ附近有黄绿色气体生成,2Cl--2e-=Cl2↑ |
| D、Ⅲ附近有无色气体生成,2H++2e-=H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com