
【题目】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,某研究小组用下图所示的实验装置,利用氢氧化钠固体、浓氨水、干冰等作原料制备氨基甲酸铵。主要反应原理:2NH3(g) + CO2(g)=H2NCOONH4(s) ΔH<0。

(1)仪器2的名称是_____________。仪器3中NaOH固体的作用是_____________。
(2)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该_____________(填“加快”、“减慢”或“不改变”)产生氨气的流速。
(3)另有一种制备氨基甲酸铵的反应器(CCl4充当惰性介质)如下图:

①若无冰水,则氨基甲酸铵易分解生成尿素[化学式为CO(NH2)2]。请写出氨基甲酸铵受热分解的化学反应方程式:_____________。
②当CCl4液体中产生较多晶体悬浮物时,即停止反 应,过滤分离得到粗产品,为了将所得粗产品干燥可采取的方法是_____________。
A.蒸馏 B.高压加热烘干 C.真空微热烘干
(4)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式为_____________。
为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验。已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案:用天平称取一定质量的样品,加水溶解,_____________,测量的数据取平均值进行计算(限选试剂:蒸馏水、澄清石灰水、BaCl2溶液)。
【答案】 三颈烧瓶 干燥氨气,防止生成的氨基甲酸铵水解 加快 H2NCOONH4![]() CO(NH2)2+H2O C NH2COONH4+2H2O=NH4HCO3+NH3·H2O 加入足量澄清石灰水,充分反应后,过滤、用蒸馏水洗涤所得沉淀、干燥后称量沉淀的质量。重复2~3次
CO(NH2)2+H2O C NH2COONH4+2H2O=NH4HCO3+NH3·H2O 加入足量澄清石灰水,充分反应后,过滤、用蒸馏水洗涤所得沉淀、干燥后称量沉淀的质量。重复2~3次
【解析】试题分析:根据装置图可知,利用装置2制备氨气,由于氨基甲酸铵易水解所以用装置3干燥氨气,利用装置4制备干燥的二氧化碳气体,在装置5中发生2NH3(g) + CO2(g)=H2NCOONH4(s)制备氨基甲酸铵。
用第二种方法制备氨基甲酸铵
①根据元素守恒可知氨基甲酸铵受热分解成尿素和水。
②氨基甲酸铵易分解,为了将所得粗产品干燥可真空微热烘干。
(4)根据元素守恒可知氨基甲酸铵和水完全水解为碳酸氢铵和氨水。
氨基甲酸铵完全水解成碳酸氢铵,与澄清石灰水反应生成碳酸钙沉淀。
解析:根据以上分析,(1)根据图示,仪器2的名称三颈烧瓶。仪器3中NaOH固体的作用是干燥氨气,防止生成的氨基甲酸铵水解。
(2)氨气易溶于稀硫酸,二氧化碳难溶于稀硫酸,若反应初期观察到装置内稀硫酸溶液中产生气泡,说明二氧化碳过量,应该加快产生氨气的流速。
(3)①根据元素守恒可知氨基甲酸铵受热分解成尿素和水,方程式为:H2NCOONH4![]() CO(NH2)2+H2O。
CO(NH2)2+H2O。
②氨基甲酸铵易分解,为了将所得粗产品干燥可真空微热烘干,故C正确;
(4)根据元素守恒可知氨基甲酸铵和水完全水解为碳酸氢铵和氨水,该反应的化学方程式为NH2COONH4+2H2O=NH4HCO3+NH3·H2O。
氨基甲酸铵完全水解成碳酸氢铵,能与澄清石灰水反应生成碳酸钙沉淀,充分反应后,过滤、用蒸馏水洗涤所得沉淀、干燥后称量沉淀的质量。重复2~3次,根据沉淀质量计算。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】3,4,5-三甲氧基苯甲醛是制备抗菌增效剂TMP的中间体,通常可以通过以下途径合成。
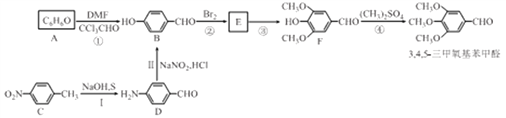
(1)写出C的名称: __________;下列说法不正确的是______________(填选项字母)。
A.反应②要控制条件防止—CHO被氧化
B.1 mol有机物F最多能与3 mol H2发生加成反应
C.有机物D不能使KMnO4溶液褪色
D.第I步所涉及的反应类型有氧化反应、还原反应
(2)有机物E的结构简式为____________,E→F的反应类型为___________反应。
(3)D与新制Cu(OH)2反应的化学方程式为__________________。
(4)满足下列条件的C的同分异构体有__________种,写出其中一种的结构简式:_____________。
①红外光谱检测表明分子中含有苯环、![]() 结构
结构
②H—NMR谱显示分子中有四种不同化学环境的氢
(5)已知:RCHO+CH3COOR'![]() RCH═CHCOOR',请结合题给信息,设计以苯酚和乙酸乙酯为原料(其他试剂任选)制备
RCH═CHCOOR',请结合题给信息,设计以苯酚和乙酸乙酯为原料(其他试剂任选)制备![]() 的合成路线:__________。
的合成路线:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,例如CO就是计入《空气质量日报》空气污染指数的项目之一。我国城市环境中的大气污染物主要是
A. CO2、Cl2、N2、SO2 B. SO2、NO2、可吸入颗粒物
C. NH3、CO2、NO2、雾 D. HCl、SO2、N2、可吸入颗粒物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。
(1)实验室在40℃、pH﹦4的条件下用Na2SO3溶液和SO2反应制取Na2S2O5:Na2SO3+SO2=Na2S2O5实验时先用CO2气体尽可能排除装置内空气的目的是_____________。
(2)若制备19 g Na2S2O5至少需标准状况下SO2_____________L。
(3)为了检验某抗氧化剂产品中Na2S2O5的质量分数,某研究小组进行如下实验:
步骤I:称取抗氧化剂产品0.2 g,将其加入到含I2浓度为0.05000 mol·L1 的100 mL稀盐酸和碘水的混合溶液中,然后加水稀释至500 mL。
步骤II:取稀释后的溶液100 mL,加入几滴淀粉溶液,用0.1000 mol·L1 Na2S2O3标准溶液进行滴定,共消耗Na2S2O3标准溶液12.00 mL(2S2O32- + I2=2I- + S4O62-)。
①写出步骤I中Na2S2O5和I2反应的离子方程式_____________。
②计算抗氧化剂产品中Na2S2O5质量分数,写出计算过程_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量的镁条分别在体积相同的①O2、②N2、③CO2中充分燃烧,所得固体的质量由大到小的正确顺序是( )
A. ①②③ B. ③②① C. ②①③ D. ②③①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列常见物质的俗名与化学式对应正确的是( )
A. 铁红——Fe3O4 B. 小苏打——Na2SO4 C. 石英——SiO2 D. 生石灰——Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值。下列说法正确的是( )
A. 向含有FeI2的溶液中通入适量氯气,当有1molFe2+被氧化时,该反应转移电子数目为3NA
B. 40gCuO和Cu2S混合物中所含铜原子的数目不等于0.5 NA
C. 含0.1molNH4HSO4的溶液中,阳离子数目略小于0.2NA
D. C3H8分子中的2个H原子分别被1个-NH2和1个-OH取代,1mol此有机物所含共用电子对数目为13NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

反应结束后,先分离出甲醇,再加人乙醚,将获得的有机层(含少量氯化氢)进行洗涤,然
后分离提纯得到产物。甲醇和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 溶解性 |
甲醇 | 64.7 | -97.8 | 易溶于水 |
3,5-二甲氧基苯酚 | 172-175 | 33-36 | 易溶于甲醇、乙醚,微溶于水 |
下列说法正确的是
A. 分离出甲醇的操作是结晶
B. 间苯三酚与苯酚互为同系物
C. 上述合成反应属于取代反应
D. 洗涤时可以用饱和Na2CO3溶液除氯化氢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com