
ĪĀ¶ČĪŖTŹ±£¬Ļņ2.0LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1.0 molPCl5£¬·“Ó¦PCl5(g) PCl3(g)£«Cl2(g)¾Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£ŗ
PCl3(g)£«Cl2(g)¾Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£ŗ
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®·“Ó¦ŌŚĒ°50 sµÄĘ½¾łĖŁĀŹĪŖv(PCl3)=0.0032 mol”¤L£1”¤s£1
B£®±£³ÖĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗāŹ±£¬c(PCl3)=0.11 mol”¤L£1,Ōņ·“Ó¦µÄ”÷H£¼0
C£®ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė1.0molPCl5”¢0.20molPCl3ŗĶ0.20molCl2£¬“ļµ½Ę½ŗāĒ°v(Õż)£¾v(Äę)
D£®ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė2.0molPCl3”¢2.0molCl2£¬“ļµ½Ę½ŗāŹ±£¬PCl3µÄ×Ŗ»ÆĀŹŠ”ÓŚ80%
C
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗA”¢øł¾Ż±ķÖŠŹż¾ŻæÉÖŖ£¬·“Ó¦½ųŠŠµ½50sŹ±Éś³ÉČżĀČ»ÆĮ×µÄĪļÖŹµÄĮæŹĒ0.16mol£¬ĘäÅØ¶ČŹĒ0.16mol”Ā2L£½0.08mol/L£¬ĖłŅŌ·“Ó¦ŌŚĒ°50 sµÄĘ½¾łĖŁĀŹĪŖv(PCl3)=0.08mol/L”Ā50s£½0.0016 mol”¤L£1”¤s£1£¬A²»ÕżČ·£»B”¢Ę½ŗāŹ±ČżĀČ»ÆĮ×µÄĪļÖŹµÄĮæÅØ¶ČŹĒ0.20mol”Ā2L£½0.10mol/L£¬±£³ÖĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗāŹ±£¬c(PCl3)=0.11 mol”¤L£1,ÕāĖµĆ÷ÉżøßĪĀ¶ČĘ½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬ŌņÕż·½Ó¦ŹĒĪüČČ·“Ó¦£¬¼“·“Ó¦µÄ”÷H£¾0£¬B²»ÕżČ·£»C”¢øł¾Ż±ķÖŠŹż¾ŻŅŌ¼°·½³ĢŹ½æÉÖŖ£¬Ę½ŗāŹ±ČżĀČ»ÆĮ×ŗĶĀČĘųµÄÅØ¶Č¾łŹĒ0.10mol/L£¬¶ųĪåĀČ»ÆĮ×µÄÅضČŌņŹĒ0.5mol/L£0.10molL£½0.40mol/L£¬ĖłŅŌøĆĪĀ¶ČĻĀĘ½ŗā³£ŹżK£½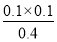 £½0.025”£ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė1.0molPCl5”¢0.20molPCl3ŗĶ0.20molCl2£¬ĘäÅØ¶Č·Ö±šŹĒ0.5mol/L”¢0.1mol/L”¢0.1mol/L£¬Ōņ“ĖŹ±
£½0.025”£ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė1.0molPCl5”¢0.20molPCl3ŗĶ0.20molCl2£¬ĘäÅØ¶Č·Ö±šŹĒ0.5mol/L”¢0.1mol/L”¢0.1mol/L£¬Ōņ“ĖŹ±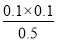 £½0.02£¼0.025£¬ÕāĖµĆ÷·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Ņņ“Ė“ļµ½Ę½ŗāĒ°v(Õż)£¾v(Äę)£¬CÕżČ·£»D”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė1.0molPCl3”¢1.0molCl2£¬ŌņĘ½ŗāŹĒµČŠ§µÄ£¬ĖłŅŌ“ļµ½Ę½ŗāŹ±£¬PCl3µÄ×Ŗ»ÆĀŹĪŖ80%”£µ«Čē¹ūĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė2.0molPCl3”¢2.0molCl2£¬ŌņĻąµ±ÓŚŹĒŌö“óŃ¹Ēæ£¬Ę½ŗāĻņÉś³ÉĪåĀČ»ÆĮ׵ķÖĪö½ųŠŠ£¬Ņņ“Ė“ļµ½Ę½ŗāŹ±£¬PCl3µÄ×Ŗ»ÆĀŹ“óÓŚ80%£¬D²»ÕżČ·£¬“š°øŃ”C”£
£½0.02£¼0.025£¬ÕāĖµĆ÷·“Ó¦ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Ņņ“Ė“ļµ½Ę½ŗāĒ°v(Õż)£¾v(Äę)£¬CÕżČ·£»D”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė1.0molPCl3”¢1.0molCl2£¬ŌņĘ½ŗāŹĒµČŠ§µÄ£¬ĖłŅŌ“ļµ½Ę½ŗāŹ±£¬PCl3µÄ×Ŗ»ÆĀŹĪŖ80%”£µ«Čē¹ūĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė2.0molPCl3”¢2.0molCl2£¬ŌņĻąµ±ÓŚŹĒŌö“óŃ¹Ēæ£¬Ę½ŗāĻņÉś³ÉĪåĀČ»ÆĮ׵ķÖĪö½ųŠŠ£¬Ņņ“Ė“ļµ½Ę½ŗāŹ±£¬PCl3µÄ×Ŗ»ÆĀŹ“óÓŚ80%£¬D²»ÕżČ·£¬“š°øŃ”C”£
æ¼µć£ŗæ¼²éæÉÄę·“Ó¦Ę½ŗā³£Źż”¢×Ŗ»ÆĀŹŅŌ¼°·“Ó¦ĖŁĀŹµÄÓŠ¹Ų¼ĘĖć£»Ķā½ēĢõ¼ž¶ŌĘ½ŗāדĢ¬µÄÓ°Ļģ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗž±±Ź”ø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
³£ĪĀĻĀ£¬ÅØ¶Č¾łĪŖ0£®1mol/L CH3COOHČÜŅŗŗĶHCNČÜŅŗµÄpH·Ö±šĪŖmŗĶn£Ø1£¼m£¼n£©”£
ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ
A£®³£ĪĀĻĀ£¬pHĻąĶ¬µÄCH3COOHČÜŅŗŗĶHCNČÜŅŗ·Ö±š¼ÓĖ®Ļ”ŹĶĻąĶ¬µÄ±¶ŹżŹ±£¬Ē°ÕßpH±ä»ÆŠ”
B£®µČĪĀĻĀ£¬µČÅØ¶ČµÄCH3COONaŗĶNaCNČÜŅŗpH£¬ŗóÕß“ó
C£®HCNČÜŅŗŗĶNaOHČÜŅŗ²»µČĢå»ż»ģŗĻŗóŅ»¶Ø“ęŌŚC£ØH+£©ØDC£ØOH-£©=C£ØCN-£©ØDC£ØNa+£©
D£®ČÜŅŗÖŠÓÉĖ®µēĄė³öµÄC£ØH+£©£¬Ē°ÕߏĒŗóÕßµÄ10m-n±¶
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗž±±Ź”¾£ĆÅŹŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÄÜĖµĆ÷“×ĖįŹĒČõµē½āÖŹµÄŹĒ
A£®ÖŠŗĶ10mL 1mol/L CH3COOHČÜŅŗŠčŅŖ10ml 1mol/L NaOHČÜŅŗ
B£®ÓĆŹ³“×æÉŅŌ³żČČĖ®ĘæÄŚµÄĖ®¹ø
C£®pH=2µÄ“×ĖįČÜŅŗĻ”ŹĶ1000±¶ŗópHŠ”ÓŚ£µ
D£®ÓĆÅØH2SO4ŗĶ“×ĖįÄĘ¹ĢĢå¹²ČČæÉÖʵƓ×Ėį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗž±±Ź”¾£ÖŻŹŠ²æ·ÖĻŲŹŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¹¤ŅµÉĻÖʱøBaCl2µÄ¹¤ŅÕĮ÷³ĢĶ¼ČēĻĀ£ŗ
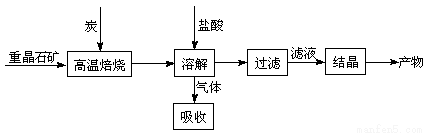
Ä³ŃŠ¾æŠ”×éŌŚŹµŃéŹŅÓĆÖŲ¾§ŹÆ£ØÖ÷ŅŖ³É·ÖBaSO4£©¶Ō¹¤Ņµ¹ż³Ģ½ųŠŠÄ£ÄāŹµŃ锣²é±ķµĆBaSO4(s) + 4C(s)  4CO(g) + BaS(s) ”÷H1£½£« 571.2 kJ”¤mol-1 ¢Ł
4CO(g) + BaS(s) ”÷H1£½£« 571.2 kJ”¤mol-1 ¢Ł
BaSO4(s) + 2C(s)  2CO2(g) + BaS(s) ”÷H2£½£« 226.2 kJ”¤mol-1 ¢Ś
2CO2(g) + BaS(s) ”÷H2£½£« 226.2 kJ”¤mol-1 ¢Ś
(1)ĘųĢåÓĆ¹żĮæNaOHČÜŅŗĪüŹÕµĆµ½Įņ»ÆÄĘ”£Ņ»¶ØÅØ¶ČµÄĮņ»ÆÄĘČÜŅŗŅņĻņæÕĘųÖŠŹĶ·Å³ōĪ¶¶ų³ĘĪŖ”°³ō¼ī”±£¬ĻĀĮŠ¶ŌÕāŅ»ĻÖĻóµÄ½āŹĶÄćČĻĪŖ×īŗĻĄķµÄŹĒ £ØĢīŠņŗÅ£©
A£®Įņ»ÆÄĘŌŚĖ®ČÜŅŗÖŠĖ®½āÉś³ÉĮĖNaOHŗĶH2SĘųĢå
B£®Įņ»ÆÄĘČÜŅŗŅņĪüŹÕæÕĘųÖŠµÄŃõĘų±»Ńõ»ÆÉś³ÉĮĖNaOH£¬Ķ¬Ź±Éś³ÉÓŠ³ōĪ¶µÄĘųĢå
C£®Įņ»ÆÄĘČÜŅŗĖ®½āµÄ¹ż³ĢÖŠŅņĪüŹÕæÕĘųÖŠµÄCO2¶ų·Å³öH2SĘųĢå
(2)ĻņĶ¬ĪļÖŹµÄĮæÅضČBaCl2ŗĶKBr»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČėAgNO3ČÜŅŗ£¬ĻČÉś³É ³Įµķ£¬µ±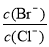 £½ Ź±£¬æŖŹ¼Éś³ÉµŚ¶žÖÖ³Įµķ£¬Ėę×ÅAgNO3ČÜŅŗµÄ½ųŅ»²½µĪ¼Ó£¬“ĖŹ±Éś³ÉµÄ³ĮµķŅŌ ĪŖÖ÷£¬ĒŅ
£½ Ź±£¬æŖŹ¼Éś³ÉµŚ¶žÖÖ³Įµķ£¬Ėę×ÅAgNO3ČÜŅŗµÄ½ųŅ»²½µĪ¼Ó£¬“ĖŹ±Éś³ÉµÄ³ĮµķŅŌ ĪŖÖ÷£¬ĒŅ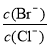 »į £ØĢī±ä“󔢱䊔”¢Ź¼ÖÕ²»±ä£©”£[ŅŃÖŖKsp(AgBr)£½5.4”Į10-13£¬Ksp(AgCl)£½2.0”Į10-10]
»į £ØĢī±ä“󔢱䊔”¢Ź¼ÖÕ²»±ä£©”£[ŅŃÖŖKsp(AgBr)£½5.4”Į10-13£¬Ksp(AgCl)£½2.0”Į10-10]
(3)·“Ó¦C(s) + CO2(g)  2CO(g)µÄ”÷H£½ kJ”¤mol-1”£
2CO(g)µÄ”÷H£½ kJ”¤mol-1”£
(4)Źµ¼ŹÉś²śÖŠ±ŲŠė¼ÓČė¹żĮæµÄĢ棬Ķ¬Ź±»¹ŅŖĶØČėæÕĘų£¬ĘäÄæµÄŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗž±±Ź”¾£ÖŻŹŠ²æ·ÖĻŲŹŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®ÓĆŪįŪöĒƼŠ×”Ņ»Š”æéĀĮ²ŌŚ¾Ę¾«µĘÉĻ¼ÓČȵ½ČŪ»Æ£¬µ«ČŪ»ÆµÄĀĮ²¢²»µĪĀ䣬ŹĒŅņĪŖĀĮ±ķĆęÉś³ÉĮĖČŪµćøüøßµÄŃõ»ÆĀĮ”£
B£®ĶŹōÓŚÖŲ½šŹō£¬ĖüµÄ»ÆѧŠŌÖŹ²»»īĘĆ£¬ĶŃĪÓŠ¶¾£¬ÄÜŹ¹µ°°×ÖŹŹ§Č„»īŠŌ£¬¹ŹĪóŹ³ĶŃĪŗó£¬Ó¦Į¢¼“·žÓĆÅ£ÄĢ»ņµ°Ēå¼±¾ČŌŁĖĶŅ½ŌŗÖĪĮĘ”£
C£®ŃĪĒÅÖŠĶس£×°ÓŠĒķÖ¬µÄKClČÜŅŗ£¬ŠĪ³ÉČēĶ¼ĖłŹ¾Ōµē³ŲµÄ±ÕŗĻ»ŲĀ·Ź±£¬ĀČĄė×ÓĻņÕż¼«ŅĘ¶Æ£¬¼ŲĄė×ÓĻņøŗ¼«ŅĘ¶Æ”£
D£®Ė®µÄµēĄėŹĒĪüČČ·“Ó¦£¬ÉżøßĪĀ¶Č£¬“Ł½ųĖ®µÄµēĄė£¬Ė®µÄĄė×Ó»ż³£ŹżKw±ä“ó”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗž±±Ź”¾£ÖŻŹŠ²æ·ÖĻŲŹŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
H2ÓėO2·¢Éś·“Ó¦µÄ¹ż³ĢÓĆÄ£ŠĶĶ¼Ź¾ČēĻĀ(”°”Ŗ”±±ķŹ¾»Æѧ¼ü)£ŗĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ

A£®¹ż³Ģ¢ńŹĒĪüČČ¹ż³Ģ
B£®¹ż³Ģ¢óŅ»¶ØŹĒ·ÅČČ¹ż³Ģ
C£®øĆ·“Ó¦¹ż³ĢĖłÓŠ¾É»Æѧ¼ü¶¼¶ĻĮŃ£¬ĒŅŠĪ³ÉĮĖŠĀ»Æѧ¼ü
D£®øĆ·“Ó¦µÄÄÜĮæ×Ŗ»ÆŠĪŹ½Ö»ÄÜŅŌČČÄܵĊĪŹ½½ųŠŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗž±±Ź”ø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
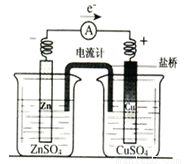
¹Ū²ģĻĀĮŠ¼øøö×°ÖĆŹ¾ŅāĶ¼£¬ÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ:
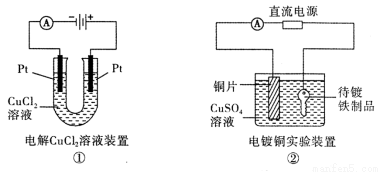
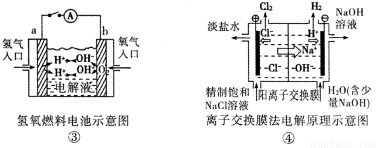
A£®×°ÖĆ¢ŁÖŠŃō¼«ÉĻĪö³öŗģÉ«¹ĢĢå
B£®×°ÖĆ¢ŚµÄ“ż¶ĘĢśÖĘĘ·Ó¦ÓėµēŌ“Õż¼«ĻąĮ¬
C£®×°ÖĆ¢Ū±ÕŗĻµē¼üŗó£¬ĶāµēĀ·µē×ÓÓÉa¼«Į÷Ļņb¼«
D£®×°ÖĆ¢ÜµÄĄė×Ó½»»»Ä¤ŌŹŠķŃōĄė×Ó”¢ŅõĄė×Ó”¢Ė®·Ö×Ó×ŌÓÉĶعż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗž±±Ź”ČżŠ£ø߶žÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŅŌ»ĘĶæó¾«æóĪŖŌĮĻ£¬ÖĘČ”½šŹōĶµÄ¹¤ŅÕČēĻĀĖłŹ¾£ŗ

¢ń£®½«»ĘĶæó¾«æó£ØÖ÷ŅŖ³É·ÖĪŖCuFeS2£¬ŗ¬ÓŠÉŁĮæCaO”¢MgO”¢Al2O3£©·ŪĖ锣
¢ņ£®²ÉÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠµē»Æѧ½ž³öŹµŃ锣½«¾«Ń”»ĘĶæó·Ū¼ÓČėµē½ā²ŪµÄŃō¼«Ēų£¬ŗćĖŁ½Į°č£¬Ź¹æó·ŪČܽā”£ŌŚŅõ¼«ĒųĶØČėŃõĘų£¬²¢¼ÓČėÉŁĮæ“߻ƼĮ”£
¢ó£®Ņ»¶ĪŹ±¼äŗ󣬳éČ”Ņõ¼«ĒųČÜŅŗ£¬ĻņĘäÖŠ¼ÓČėÓŠ»śŻĶČ”¼Į(RH)·¢Éś·“Ó¦£ŗ2RH(ÓŠ»śĻą)+Cu2+(Ė®Ļą) R2Cu(ÓŠ»śĻą)+2H£«(Ė®Ļą)·ÖĄė³öÓŠ»śĻą£¬ĻņĘäÖŠ¼ÓČėŅ»¶ØÅØ¶ČµÄĮņĖį£¬Ź¹Cu2+µĆŅŌŌŁÉś”£ ¢ō£®µē½āĮņĖįĶČÜŅŗÖĘµĆ½šŹōĶ”£
R2Cu(ÓŠ»śĻą)+2H£«(Ė®Ļą)·ÖĄė³öÓŠ»śĻą£¬ĻņĘäÖŠ¼ÓČėŅ»¶ØÅØ¶ČµÄĮņĖį£¬Ź¹Cu2+µĆŅŌŌŁÉś”£ ¢ō£®µē½āĮņĖįĶČÜŅŗÖĘµĆ½šŹōĶ”£
£Ø1£©»ĘĶæó·Ū¼ÓČėŃō¼«ĒųÓėĮņĖį¼°ĮņĖįĢśÖ÷ŅŖ·¢ÉśŅŌĻĀ·“Ó¦£ŗCuFeS2 + 4H+£½Cu2+ + Fe2+ + 2H2S”ü 2Fe3+ + H2S£½2Fe2+ + S”ż+ 2H+ £¬Ńō¼«ĒųĮņĖįĢśµÄÖ÷ŅŖ×÷ÓĆŹĒ ”££Ø2£©Ņõ¼«Ēų£¬µē¼«ÉĻæŖŹ¼Ź±ÓŠ“óĮæĘųÅŻ²śÉś£¬ŗóÓŠŗģÉ«¹ĢĢåĪö³ö£¬Ņ»¶ĪŹ±¼äŗóŗģÉ«¹ĢĢåČܽā”£Š“³öĪö³öŗģÉ«¹ĢĢåµÄ·“Ó¦·½³ĢŹ½ ”£
£Ø3£©ČōŌŚŹµŃéŹŅ½ųŠŠ²½Öč¢ó£¬·ÖĄėÓŠ»śĻąŗĶĖ®ĻąµÄÖ÷ŅŖŹµŃéŅĒĘ÷ŹĒ ”£
£Ø4£©²½Öč¢ó£¬ĻņÓŠ»śĻąÖŠ¼ÓČėŅ»¶ØÅØ¶ČµÄĮņĖį£¬Cu2+µĆŅŌŌŁÉśµÄŌĄķŹĒ ”££Ø5£©²½Öč¢ō£¬Čōµē½ā200mL0.5 mol/LµÄCuSO4ČÜŅŗ£¬Éś³ÉĶ3.2 g£¬“ĖŹ±ČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģÕć½Ź”ø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
115”ćCŹ±£¬Į½ÖÖĘųĢ¬ĢžŅŌČĪŅā±ČĄż»ģŗĻ£¬1 L»ģŗĻĢžŌŁÓė9 LŃõĘų»ģŗĻ£¬³ä·ÖČ¼ÉÕŗó»Öø“µ½ŌדĢ¬£¬ĖłµĆĘųĢåĢå»żČŌŹĒ10 L”£ĻĀĮŠø÷×é»ģŗĻĢž²»·ūŗĻ“ĖĢõ¼žµÄŹĒ
A£®CH4ŗĶC2H4 B£®CH4ŗĶC3H4 C£®C2H4ŗĶC3H4 D£®C2H2ŗĶC3H6
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com