
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3molA、2molB | 6molA、4molB | 2molC |
| 达到平衡的时间/min | 5 | 8 | |
| A的浓度/mol•L-1 | C1 | C2 | |
| C的体积分数/% | ω1 | ω3 | |
| 混合气体的密度/g•L-1 | ρ1 | ρ2 |
| A. | 若 x<4,2C1<C2 | |
| B. | 容器甲达到平衡所需的时间比容器乙达到平衡所需的时间短 | |
| C. | 无论x的值是多少,均有2ρ1=ρ2 | |
| D. | 若 x=4,则ω1=ω3 |
分析 A.恒温恒容下,乙等效为在甲中平衡基础上压强增大一倍,若x<4,则正反应为气体体积减小的反应,平衡正向移动,则乙中反应物转化率高于A中反应物转化率;
B.起始浓度越大,反应速率越快,则到达平衡时间越短;
C.起始乙中同种物质的投入量是甲的2倍,根据质量守恒定律知,乙中气体质量为甲中2倍,容器的容积相等;
D.若x=4,反应前后气体的体积不变,开始只投入C与起始投料比n(A):n(B)=3:1为等效平衡,平衡时同种物质的含量相等,甲中起始投料比为3:2,等效为在起始投料比n(A):n(B)=3:1的基础上再加入1份的B,平衡正向移动,平衡正向移动,B的转化率降低,B的含量增大,A的含量减低,C的含量不能确定.
解答 解:A.恒温恒容下,乙等效为在甲中平衡基础上压强增大一倍,若x<4,则正反应为气体体积减小的反应,平衡正向移动,则乙中反应物转化率高于A中反应物转化率,则2C1>C2,故A错误;
B.乙中起始浓度越大,反应速率越快,到达平衡时间更短,所以容器甲达到平衡所需的时间比容器乙达到平衡所需的时间长,故B错误;
C.起始乙中同种物质的投入量是甲的2倍,根据质量守恒定律知,乙中气体质量为甲中2倍,容器的容积相等,则一定存在2ρ1=ρ2,故C正确;
D.若x=4,反应前后气体的体积不变,开始只投入C与起始投料比n(A):n(B)=3:1为等效平衡,平衡时同种物质的含量相等,甲中起始投料比为3:2,等效为在起始投料比n(A):n(B)=3:1的基础上再加入1份的B,平衡正向移动,B的转化率降低,B的含量增大,A的含量减低,C的含量不能确定,故D错误;
故选C.
点评 本题考查化学平衡的计算,题目难度中等,涉及等效平衡的判断、化学平衡及其影响化学反应速率、转化率等知识,注意判断等效平衡为解答关键,注意掌握化学平衡及其影响,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 正反应是放热反应的可逆反应,升高温度v(正)>v(逆) | |
| B. | 加压可使速率加快,是因为增加活化分子百分数而使反应速率加快 | |
| C. | 活化分子的碰撞不一定都能发生化学反应 | |
| D. | 催化剂可改变反应进程,故加催化剂改变了一个反应的△H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol | B. | 3mol | C. | 4mol | D. | 6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
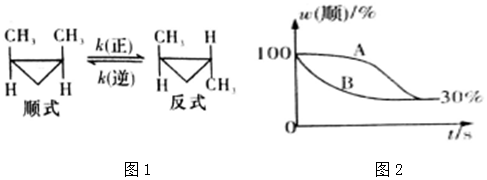
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].
N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].查看答案和解析>>
科目:高中化学 来源: 题型:实验题
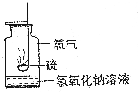 郑州一中是一所具有丰厚的历史积淀、独特的精神内涵,以关注学生智慧与灵魂为学校文化内核,充满创新精神,能够培养具有国际视野的拔尖人才,拥有核心竞争力的国内名校.目前一中教育集团包含小学部、初中部、高中部三个学部的十余所学校.学校以主体课堂教学为载体,以培养学生的创新思维和实践能力为目标,在教学活动中特别注重学生科学素养的提升,如对于I A和ⅥA族重要元素化合物的性质,各校区根据实际情况开展了丰富多彩的探究活动.
郑州一中是一所具有丰厚的历史积淀、独特的精神内涵,以关注学生智慧与灵魂为学校文化内核,充满创新精神,能够培养具有国际视野的拔尖人才,拥有核心竞争力的国内名校.目前一中教育集团包含小学部、初中部、高中部三个学部的十余所学校.学校以主体课堂教学为载体,以培养学生的创新思维和实践能力为目标,在教学活动中特别注重学生科学素养的提升,如对于I A和ⅥA族重要元素化合物的性质,各校区根据实际情况开展了丰富多彩的探究活动. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强p/100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁制品的腐蚀常以析氢腐蚀为主 | |
| B. | 厨房中常用碳酸钠溶液洗涤餐具上的油污 | |
| C. | 明矾[KAl(SO4)2•12H2O]用于水的杀菌消毒 | |
| D. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | H2C2O4溶液 | KMnO4溶液 | 温度 |
| Ⅰ | 20mL 0.2mol•L-1 | 30mL 0.01mol•L-1 | 25℃ |
| Ⅱ | 20mL 0.1mol•L-1 | 30mL 0.01mol•L-1 | 25℃ |
| Ⅲ | 20mL 0.2mol•L-1 | 30mL 0.01mol•L-1 | 50℃ |
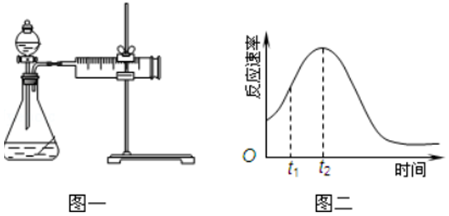
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com