
 常温下用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1CH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )
常温下用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1CH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10)溶液所得滴定曲线如图.下列说法正确的是( )| A. | 曲线I和曲线II分别代表的是CH3COOH和HCN | |
| B. | 点③和点⑤所示溶液中由水电离出的c(H+):⑤>③ | |
| C. | 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) | |
| D. | 在点②和③之间(不包括端点)存在关系:c(Na+)>c(A-)>c(H+)>c(OH-) (A-代表溶液中的酸根离子) |
分析 常温下用0.10mol/LNaOH溶液分别滴定20.00mL浓度均为0.10mol/LCH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10),对于同浓度同体积的CH3COOH和HCN来说,根据电离平衡常数可判断酸性CH3COOH>HCN,结合图象和溶液中的守恒思想,据此判断分析.
解答 解:常温下用0.10mol/LNaOH溶液分别滴定20.00mL浓度均为0.10mol/LCH3COOH(Ka=1.75×10-5)溶液和HCN(Ka=4.9×10-10),对于同浓度同体积的CH3COOH和HCN来说,根据电离平衡常数可判断酸性CH3COOH>HCN,
A.酸性CH3COOH>HCN,HCN电离出的H+更少,pH值更大,则起始时,在pH图象上,起点更高的是HCN,因此曲线I是HCN,曲线II是CH3COOH,故A错误;
B.点③和点⑤表示的溶液中,溶液均为中性,则溶液中c(H+)=c(OH-),对于I,溶液中存在HCN和NaCN,对于II,溶液中存在CH3COONa和CH3COOH,根据图象,I溶液中此时NaOH溶液的量是很少的,意味着溶液中大量存在HCN,II溶液中所加的NaOH溶液体积几乎接近20.00mL,溶液中大量存在的是CH3COONa,HCN大量存在抑制水的电离,CH3COONa大量存在,水解促进水的电离,则点③和点⑤所示溶液中由水电离出的c(H+):⑤<③,故B错误;
C.点①和点②所示溶液中,所加NaOH溶液的体积均为10.00mL,I溶液的组分为NaCN和HCN的起始量为1:1,II溶液的组分为CH3COONa和CH3COOH的起始量为1:1,分别对于I溶液和II溶液,有物料守恒,I:2c(Na+)=c(CN-)+c(HCN)=$\frac{1}{15}$mol/L,II:2c(Na+)=c(CH3COOH)+c(CH3COO-)=$\frac{1}{15}$mol/L,则c(CN-)+c(HCN)=c(CH3COOH)+c(CH3COO-),因此c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH),故C正确;
D.在点②和③之间(不包括端点),根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(A-),根据图象,溶液一直是酸性,则c(H+)>c(OH-),因此溶液中c(Na+)<c(A-),故D错误.
故选C.
点评 本题考查酸碱滴定原理,弱电解质的电离平衡,盐类水解得知识,根据图象分析,牢牢把握溶液中的守恒思想是解题的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
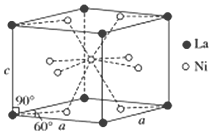 钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
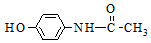
| A. | 1mol该物质最多消耗2molNaOH | B. | 该物质的分子式为C8H8NO2 | ||
| C. | 该物质能发生取代反应和加成反应 | D. | 该物质苯环上的一溴代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜屑加入 Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 将氯化亚铁酸性溶液和H2O2混合:Fe2++2H++H2O2═Fe3++2H2O | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氯化银可溶于氨水 | |
| B. | 银氨溶液中加入少量氯化钠有白色沉淀 | |
| C. | 银氨溶液中加入盐酸有白色沉淀 | |
| D. | 银氨溶液可在酸性条件下稳定存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
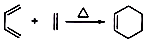 ,
,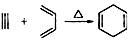 叫狄尔斯阿德而反应,用 于构建六元环,则下列说法不正确的是( )
叫狄尔斯阿德而反应,用 于构建六元环,则下列说法不正确的是( )| A. | 狄尔斯阿德而反应为加成反应,原子利用率为100% | |
| B. | 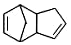 可通过狄尔斯阿德而反应合成,而 可通过狄尔斯阿德而反应合成,而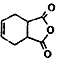 不可通过狄尔斯阿德而反应合成 不可通过狄尔斯阿德而反应合成 | |
| C. | 2-甲基-1,3-丁二烯和丙炔发生上述反应产物有两种 | |
| D. |  可由环戊二烯与丙烯酸甲酯发生上述反应得到 可由环戊二烯与丙烯酸甲酯发生上述反应得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和浓硝酸为原料生产硝酸铜 | B. | 甲烷与氯气制备一氯甲烷 | ||
| C. | 由反应2SO2+O2?2SO3制SO3 | D. | 乙烯与HBr制取溴乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| 测定上述实验用的Fe(NO3)3溶液的pH 配制相同pH的稀硝酸 溶液,并将适量此溶液加入有银镜的试管内. | 若银镜消失,假设2成立. 若银镜不消失,假设2不成立. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/s | 0 | 10 | 20 | 30 | 40 |
| n(SO3)/mol | 0 | 0.6 | 1.0 | 1.2 | 1.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com