
| A.在催化剂存在的条件下,苯和溴水发生反应可生成无色、比水重的液体溴苯。 |
| B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验。 |
| C.醇中含有少量水可加入生石灰再蒸馏制得无水乙醇。 |
| D.有朝一日宇航员乘坐“嫦娥”遨游月空时,在其轨道舱中无法完成“粗盐的提纯”实验 |
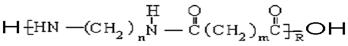 的单体为___________
的单体为___________ 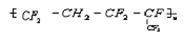 合成它的单体为________________________
合成它的单体为________________________科目:高中化学 来源:不详 题型:实验题
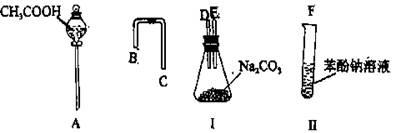
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
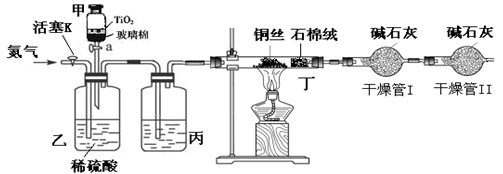
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

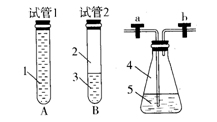
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
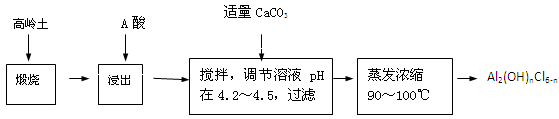
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.KI淀粉溶液中通入Cl2,溶液变蓝原因是淀粉能与Cl2发生显色反应 |
| B.浓硝酸在光照条件下变黄是由于浓硝酸不稳定,生成有色物质能溶于浓硝酸 |
| C.某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成说明该溶液中含有SO42- |
| D.常温下,浓硫酸可储存在铁质或铝制器皿中说明常温下铁和铝与浓硫酸不反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
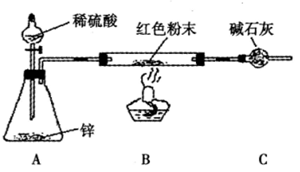
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验内容 | 实验的异常情况 | 原因分析 |
| A | 制备Fe(OH)2 | 观察不到白色沉淀 | 可能原料中的Fe2+被氧化或未隔绝空气 |
| B | 蒸发结晶 | 蒸发皿破裂 | 酒精灯灯芯碰到热的蒸发皿底部或蒸发到剩少量液体时继续加热 |
| C | 分离水和CCl4 | 打开分液漏斗活塞后,下层液体难以流出 | 没有装漏斗上塞子拔掉或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐 |
| D | 点燃法除去CO2中的CO杂质 | 无法点燃 | CO的着火点较高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 测定序号 | 待测溶液的体积/mL | 所耗盐酸标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com