
| A. | 常温下二者都可用铁制容器贮存 | B. | 常温下二者都能与铜较快反应 | ||
| C. | 露置于空气中,溶液浓度均降低 | D. | 浓HNO3与浓H2SO4都具有强氧化性 |
科目:高中化学 来源: 题型:解答题
| 族周 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
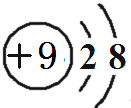 .元素①的最高价氧化物的电子式:
.元素①的最高价氧化物的电子式: ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑥ | B. | ②③④⑤ | C. | ④⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅可用来制造石英光导纤维 | |
| B. | 亚硫酸钠可用于防止食品氧化变质,延长食品的保质期 | |
| C. | 碳酸氢钠俗名苏打,可用于制作发酵粉和治疗胃酸过多的药物 | |
| D. | 三氧化二铁常用作红色油漆和涂料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
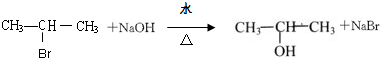
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na>Mg>Al>Zn>Fe | B. | Al>Mg>Na>Fe>Zn | C. | Mg>Al>Na>Zn>Fe | D. | Zn>Fe Na>Mg>Al> |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com