
ĻĀĮŠÓŠ¹ŲÄÜĮæµÄÅŠ¶Ļ»ņ±ķŹ¾·½·ØÕżČ·µÄŹĒ
A£®“ÓC(ŹÆÄ«)£½C(½šøÕŹÆ) ¦¤H£½1£®9 kJ”¤mol£1£¬æÉÖŖ½šøÕŹÆ±ČŹÆÄ«øüĪȶØ
B£®µČÖŹĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ŗóÕ߷ųöČČĮæøü¶ą
C£®ÓÉH+(aq)£«OH£(aq)£½H2O(l) ¦¤H£½-57£®3 kJ”¤mol£1£¬ŌņĻņŗ¬0£®1 mol HClµÄŃĪĖįÖŠ¼ÓČė4£®0 gNaOH¹ĢĢ壬·Å³öČČĮæµČÓŚ5£®73 kJ
D£®Ķ¬Ņ»øö»Æѧ·“Ó¦£¬»Æѧ¼ĘĮæŹż²»Ķ¬£¬¦¤HµÄÖµ²»Ķ¬£»»Æѧ¼ĘĮæŹżĻąĶ¬¶ųדĢ¬²»Ķ¬£¬¦¤HµÄÖµŅ²²»Ķ¬”£
D
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗĪļÖŹĖłŗ¬ÄÜĮæŌ½µĶŌ½ĪČ¶Ø£¬½šøÕŹÆ±ČŹÆÄ«ÄÜĮæøߣ¬ŹÆÄ«±Č½šøÕŹÆĪČ¶Ø£¬¹ŹAĻī“ķĪó£»µČÖŹĮæµÄĮņÕōĘų±ČĮņ¹ĢĢåÄÜĮæøߣ¬µČÖŹĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ŗóÕ߷ųöČČĮæÉŁ£¬¹ŹB“ķĪó£»ĒāŃõ»ÆÄĘ¹ĢĢåČÜÓŚĖ®·ÅČČ£¬Ļņŗ¬0£®1 mol HClµÄŃĪĖįÖŠ¼ÓČė4£®0 gNaOH¹ĢĢ壬·Å³öČČĮæ“óÓŚ5£®73 kJ£¬¹ŹC“ķĪó£»”£¦¤HµÄÖµÓė»Æѧ¼ĘĮæŹż¶ŌÓ¦£¬¹ŹDÕżČ·”£
æ¼µć£ŗ±¾Ģā漲鷓ӦČČ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”ŗ¼ÖŻŹŠø߶ž10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÄųļÓ£ØNiCd£©æɳäµēµē³ŲŌŚĻÖ“śÉś»īÖŠÓŠ¹ć·ŗÓ¦ÓĆ”£ŅŃÖŖijÄųļÓµē³ŲµÄµē½āÖŹČÜŅŗĪŖKOHČÜŅŗ£¬Ęä³ä”¢·Åµē°“ĻĀŹ½½ųŠŠ:
Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
ÓŠ¹ŲøƵē³ŲµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®³äµēŹ±Ńō¼«·“Ó¦:Ni(OH)2-e-+OH-====NiOOH+H2O
B£®³äµē¹ż³ĢŹĒ»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵĹż³Ģ
C£®·ÅµēŹ±øŗ¼«ø½½üČÜŅŗµÄ¼īŠŌ²»±ä
D£®·ÅµēŹ±µē½āÖŹČÜŅŗÖŠµÄOH-ĻņÕż¼«ŅʶÆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”ŗ¼ÖŻŹŠøßŅ»10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬ĻąĶ¬Ģå»żµÄĪļÖŹ£¬ĖüĆĒµÄĪļÖŹµÄĮæŅ»¶ØĻąµČ
B£®ČĪŗĪĢõ¼žĻĀ£¬µČĪļÖŹµÄĮæµÄ¶žŃõ»ÆĮņŗĶŅ»Ńõ»ÆĢ¼Ėłŗ¬µÄ·Ö×ÓŹżŅ»¶ØĻąµČ
C£®1LŅ»Ńõ»ÆĢ¼ĘųĢåŅ»¶Ø±Č1LŃõĘųµÄÖŹĮ抔
D£®µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄĒæĖįÖŠĖłŗ¬µÄH+ŹżŅ»¶ØĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”ø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖĻĀĮŠĮ½ÖÖĘųĢ¬ĪļÖŹÖ®¼äµÄ·“Ó¦£ŗ
C2H2(g)£«H2(g) ==?C2H4(g) ¢Ł
2CH4(g) == C2H4(g)£«2H2(g) ¢Ś
ŅŃÖŖŌŚ½µµĶĪĀ¶ČŹ±¢ŁŹ½Ę½ŗāĻņÓŅŅĘ¶Æ£¬¢ŚŹ½Ę½ŗāĻņ×óŅĘ¶Æ£¬ŌņĻĀĮŠČżøö·“Ó¦£ŗ
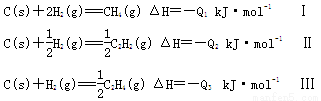
(Q1”¢Q2”¢Q3¾łĪŖÕżÖµ)£¬”°QÖµ”±“óŠ”±Č½ĻÕżČ·µÄŹĒ
A£®Q2>Q1>Q3 B£®Q1>Q2>Q3
C£®Q1>Q3>Q2 D£®Q3>Q1>Q2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”ø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ£ŗC(s)+H2O(g) CO(g)+H2(g) ¦¤H = +130 kJ”¤mol-1
CO(g)+H2(g) ¦¤H = +130 kJ”¤mol-1
2C(s)+O2(g) 2CO(g) ¦¤H=a kJ”¤mol-1
2CO(g) ¦¤H=a kJ”¤mol-1
H”ŖH”¢O OŗĶO”ŖH¼üµÄ¼üÄÜ·Ö±šĪŖ436 kJ”¤mol-1”¢496 kJ”¤mol-1ŗĶ462 kJ”¤mol-1,ŌņaĪŖ
OŗĶO”ŖH¼üµÄ¼üÄÜ·Ö±šĪŖ436 kJ”¤mol-1”¢496 kJ”¤mol-1ŗĶ462 kJ”¤mol-1,ŌņaĪŖ
A£®-332 B£®-118 C£®-220 D£®+350
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”ø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®¶ĘĶĢśÖĘĘ·¶Ę²ćŹÜĖšŗó£¬ĢśÖĘĘ·±ČŹÜĖšĒ°øüČŻŅ×ÉśŠā
B£®ĶµÄ½šŹō»īĘĆŠŌ±ČĢśµÄČõ£¬æÉŌŚŗ£ĀÖĶāæĒÉĻ×°ČōøÉĶæéŅŌ¼õ»ŗĘäøÆŹ“
C£®Ē¦Šīµē³Ų·ÅµēŹ±µÄøŗ¼«ŗĶ³äµēŹ±µÄŃō¼«¾ł·¢Éś»¹Ō·“Ó¦
D£®ŌŚ³±ŹŖµÄ¼īŠŌ»·¾³ÖŠ£¬½šŹōµÄµē»ÆѧøÆŹ“Ö÷ŅŖŹĒĪöĒāøÆŹ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”¶«ŃōĶā¹śÓļѧŠ£ø߶žÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚŅ»¶ØĢå»żpH=12µÄBa(OH)2ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄNaHSO4ČÜŅŗ£¬µ±ČÜŅŗÖŠµÄBa2£«Ē”ŗĆĶźČ«³ĮµķŹ±£¬ČÜŅŗpH=11”£Čō·“Ó¦ŗóČÜŅŗµÄĢå»żµČÓŚBa(OH)2ČÜŅŗÓėNaHSO4ČÜŅŗµÄĢå»żÖ®ŗĶ£¬ŌņBa(OH)2ČÜŅŗÓėNaHSO4ČÜŅŗµÄĢå»ż±ČŹĒ
A£®1”Ć9 B£®1”Ć1 C£®1”Ć2 D£®1”Ć4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”¶«ŃōĶā¹śÓļѧŠ£ø߶žÉĻѧʌʌ֊»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Óė“æĖ®µÄµēĄėĻąĖĘ£¬Ņŗ°±ÖŠŅ²“ęŌŚ×ÅĪ¢ČõµÄµēĄė£ŗ2NH3  NH4++NH2-ŅŌĻĀŠšŹöÖŠ“ķĪóµÄŹĒ
NH4++NH2-ŅŌĻĀŠšŹöÖŠ“ķĪóµÄŹĒ
A£®Ņŗ°±ÖŠŗ¬ÓŠNH3”¢NH4+”¢NH2-µČĪ¢Į£
B£®Ņ»¶ØĪĀ¶ČĻĀŅŗ°±ÖŠC(NH4+)”¤C(NH2-)ŹĒŅ»øö³£Źż
C£®Ņŗ°±µÄµēĄė“ļµ½Ę½ŗāŹ±C(NH3) = C(NH4+) = C(NH2-)
D£®Ö»ŅŖ²»¼ÓČėĘäĖūĪļÖŹ£¬Ņŗ°±ÖŠC(NH4+) = C(NH2-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗÓÄĻŪ³ĮźĻŲµŚŅ»øßÖŠø߶žÉĻµŚŅ»“Īæ¼ŹŌ»Æѧ£ØB£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«ĘųĢåXŗĶĘųĢåYø÷0.16mol³äČė10LŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦
X(g)£«Y(g) 2Z(g) ¦¤H£¼0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£¬·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ
2Z(g) ¦¤H£¼0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£¬·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ
±ķ£ŗ
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®øĆĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK£½1.44
B£®ĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Č£¬·“Ó¦“ļµ½ŠĀĘ½ŗāĒ°¦Ķ(Äę)£¾¦Ķ(Õż)
C£®·“Ó¦Ē°2minµÄĘ½¾łĖŁĀŹ¦Ķ(Z)£½2.0”Į10£3mol”¤L£1”¤min-1
D£®ĘäĖūĢõ¼ž²»±ä£¬ŌŁ³äČė0.2mol Z£¬Ę½ŗāŹ±XµÄĢå»ż·ÖŹżŌö“ó
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com