
A、14g分子通式为CnH2n的链烃中含有的C═C的数目为
| ||
| B、标准状况下,NO和 O2各11.2L 混合,所得混合气体的分子总数为 0.75NA | ||
| C、25℃时,pH=7的NH4Cl和NH3?H2O混合溶液中,OH-离子数为10-7NA | ||
| D、两份2.7g铝分别与100mL浓度为2mol?L-1的盐酸和氢氧化钠溶液充分反应,转移的电子数均为0.3NA |
| 14g |
| 14ng/mol |
| 1 |
| n |
| 1 |
| n |
| 14g |
| 14ng/mol |
| 1 |
| n |
| 1 |
| n |
| NA |
| n |
| 11.2L |
| 22.4L/mol |
| 2.7g |
| 27g/mol |


科目:高中化学 来源: 题型:
| A、人口增多→空气中CO2浓度增大→空气酸度大幅增加 |
| B、含磷洗衣粉→水体富营养化→水栖生物大量死亡 |
| C、汽车尾气→光化学污染→咳嗽和气喘者增多 |
| D、氟氯烃→臭氧空洞→皮肤癌患者增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S(s)的能量高于SO2(g)的能量 |
| B、S(s)和O2(g)的总能量大于SO2(g)的能量 |
| C、若有S(g)+O2(g)=SO2(g)△H2,则△H2>△H1 |
| D、形成1mol SO2(g)的化学键释放的总能量比断裂1mol S(s)和1mol O2(g)的化学键所吸收的总能量多297.23kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠和氧气反应,条件不同,产物不同 |
| B、钠钾合金通常状况下呈液态,可作原子反应堆的导热剂 |
| C、钠的化学活泼性很强,少量的钠可保存在有机溶剂CCl4中 |
| D、由于钠比较活泼,所以它能从盐的熔融物中置换出金属活动顺序表中钠后面的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.5mol/(L?s ) |
| B、v(C)=6.0mol/(L?min) |
| C、v(B)=0.6mol/(L?s) |
| D、v(D)=0.4mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
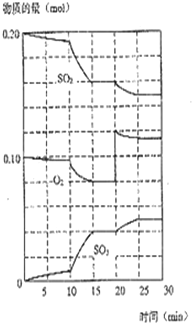 在一定条件下,二氧化硫和氧气发生如下反应:
在一定条件下,二氧化硫和氧气发生如下反应:| 催化剂 |
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com