
����Ŀ����Ũ��SO2�����Ĵ����ǹ�ҵ���⣬��ҵ�ϳ����÷ϼ�������Ҫ�ɷ�Na2CO3���������᳧β���е�SO2�Ʊ���ˮNa2SO3�ijɱ��ͣ��������ԣ����������¡�
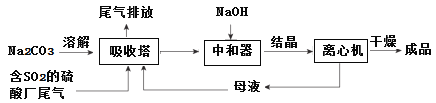
��1��Ϊ��ʹSO2������������ȫ���ڲ��ı�����������������£����Բ�ȡ�ĺ�
����ʩ______________��_______________����д��������
��2���к����з�������Ҫ��Ӧ�����ӷ���ʽ��_____________________��
��3����ͼΪ��������Na2CO3��Һ��SO2��Ӧ��������Һ��ɱ仯��
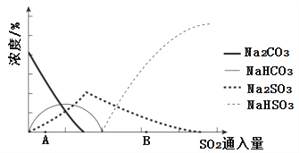
������ڷ�Ӧ��ͼ��A����ǰ���Ļ�ѧ����ʽ��__________________��
��ͨ����ⷨ�ɷ���ͼ��B��NaHSO3��Na2SO3����ʵ��Na2SO3��ѭ�����ã�ʾ��ͼ���£�
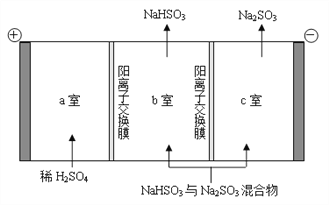
��������NaHSO3��Na2SO3������ԭ��___________________��
��4����ͼ���������Ƶ��ܽ�����ߣ��¶���33��ǰ���Ӧ��ͬ���ʣ�������˵����ȷ����______
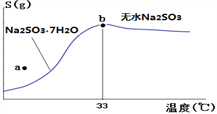
A��a��ʱ��ҺΪ��������Һ
B��b��ʱNa2SO3��7H2O����ˮNa2SO3����
C���Ʊ���ˮNa2SO3��Ӧ����95~100�����Ũ������ȴ�����½ᾧ
��5������ú������ʵ������ʵ����и���Һ�ֱ�����SO2��������������������__________
A��Na2SO3 B��Na2S C��Ba(NO3)2 D������KMnO4
���𰸡�����SO2��������Na2CO3��Һ��Ũ�ȣ��ʵ����¡�������Һ�����������ܷ���Na2CO3��Һ�����Ⱥ������ɣ�HSO3- + OH- = SO32- + H2O 2Na2CO3 + SO2 + H2O =2 NaHCO3 + Na2SO3����4OH��-4e��=2H2O+O2����c(H+)����H����a�Ҿ������ӽ���Ĥ����b�ң�H����SO32�� �������HSO3����Na2SO3ת��ΪNaHSO3������2H��-2e��=H2��������HSO3��![]() H��+ SO32�������ƶ���Na����b�ҽ���c�ң�NaHSO3ת��ΪNa2SO3��BC
H��+ SO32�������ƶ���Na����b�ҽ���c�ң�NaHSO3ת��ΪNa2SO3��BC
����������1���ô�����Һ���պ���SO2��β��������ͨ������SO2���١�����Na2CO3��Һ��Ũ�ȡ�������Һ�����������ܷ���Na2CO3��Һ�����ȴ�ʩʹSO2������������ȫ��
��2�����Ŷ�������ͨ����������������Ҫ�ǵõ����������ƣ��к�������Ҫ�ǽ�����������ת��Ϊ�����ƣ�ͬʱ̼�����Ʒ�Ӧ�õ�̼���ƣ���Ҫ��Ӧ��ѧ����ʽΪ��NaHSO3+NaOH=Na2SO3+H2O����Ӧ�����ӷ���ʽΪHSO3- + OH- = SO32- + H2O��
��3������ͼ��֪�����ڷ�Ӧ��ͼ��A����ǰ��̼�������������Ӧ����̼���������������ƣ���Ӧ����ʽΪ2Na2CO3 + SO2 + H2O =2 NaHCO3 + Na2SO3 -��
��ͨ����ⷨ�ɷ���NaHSO3��Na2SO3��������2H2O-4e-=4H++O2����c��H+������H+��a�Ҿ������ӽ���Ĥ����b�ң�H+��SO32-�������HSO3-��Na2SO3ת��ΪNaHSO3������2H+-2e-=H2��������HSO3-![]() H++SO32-�����ƶ���Na+��b�ҽ���c�ң�NaHSO3ת��ΪNa2SO3��ʵ��Na2SO3��ѭ�����ã�
H++SO32-�����ƶ���Na+��b�ҽ���c�ң�NaHSO3ת��ΪNa2SO3��ʵ��Na2SO3��ѭ�����ã�
��4��A��a�����ܽ�������Ϸ�����ʱ��ҺΪ��������Һ���ڶ�Ӧ�¶��»��о�����������A����B����b�������ľ��������Na2SO3��7H2O����ˮNa2SO3�Ļ������߹��棬��B��ȷ�� C�����Ʊ���ˮNa2SO3��Ӧ����95~100������Ũ�����ᾧ�������ȹ��ˣ�������ȴ�ᾧ����C����ΪB��
��5������ú������ʵ������ʵ����и���Һ�ֱ�������SO2��
A��Na2SO3 ���ն����������ķ�ӦΪ��Na2SO3+SO2+H2O=2NaHSO3��1molNa2SO3 ������ն�������1mol��B��Na2S���ն����������ķ�ӦΪ��2Na2S+5SO2+2H2O=4NaHSO3+3S����1mol2Na2S��෴Ӧ��������2.5mol��C��Ba��NO3��2���ն�������Ӧ��ѧ����ʽΪBa��NO3��2+3SO2+2H2O=BaSO4��+2H2SO4+2NO����1molBa��NO3��2������ն�������3mol��D������KMnO4��Һ���ն�������ķ�Ӧ2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+��1molKMnO4��෴Ӧ��������2.5mol����ΪC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�� A��������Ԫ����ɵĻ����ij�о�С�鰴��ͼ����̽������ɣ�
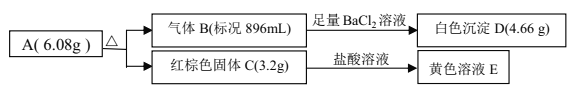
��ش�
��1��д������ɫ���� C �Ļ�ѧʽ____________��
��2��д�� A ���ȷֽⷴӦ�Ļ�ѧ����ʽ____________��
��3��д������ B ����Һ E ��Ӧ�����ӷ���ʽ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ѱۣ����ʯ���� TiO2�����㷺�����������ɫ���ᡣ��ҵ������������Ҫ�ɷ�Ϊ FeTiO3������ Fe2O3 �� SiO2 �����ʣ�Ϊԭ�����Ѱ۵���Ҫ�������£�
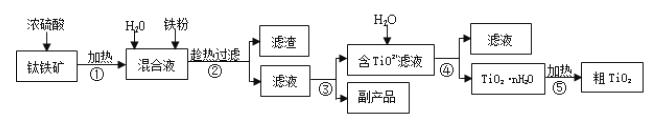
�ش��������⣺
��1���ڢڲ����������ijɷ���________��
��2������������Ҫ�����������γ� TiO2��nH2O �ܽ����ù��չ�����Ҫ��ʵ��������ɣ����еġ����ˡ���������ѡ������װ��________����ѡ���
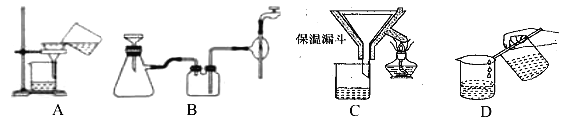
��3���ڢ۲���ʵ�������______�����ˣ��Ӷ���ø���Ʒ FeSO4��7H2O��
��4��Ϊ�ⶨ������������Һ��TiO2+��Ũ�ȣ�ȡ������Һ10 mL ������ˮϡ����100 mL������������ۣ������ʹ����ȫ��Ӧ��3TiO2+ + Al + 6H+ = 3Ti3+ + Al3+ + 3H2O�����˺�ȡ����Һ20.00 mL��������ʱ������Һ����ı仯���Բ��ƣ��������еμ�2��3 ��KSCN��Һ��ָʾ������ 0.1000 mol��L-1NH4Fe(SO4)2 ����Һ�ζ�����Һ���ֺ�ɫ����ʱ��Һ�� Ti3+ȫ��������Ϊ Ti4+�����ı�Һ30.00mL���ش��������⣺
�����в�����ʹ���� TiO2+Ũ��ƫ�ߵ���______��
A. �����Ʊ�Һ�Ĺ����У�δϴ���ձ��Ͳ�����
B. �����Ʊ�Һ�����Ǹ��ӿ̶���
C��������ˮϴ�Ӻ�δ����ϴ�ĵζ���ȡ����Һ
D���ڵζ��յ����ʱ���ӵζ��̶ܿ���
����ô�����Һ�� TiO2+�����ʵ���Ũ����______��
��5����ѧ�Ҵӵ��ұ�����Ĺ����еõ��������ҳ���ұ���ѵ��¹��ա�TiO2 ֱ�ӵ�ⷨ�����ѣ������Ϊ���ڵ��Ȼ��ƣ�ԭ����ͼ��ʾ��
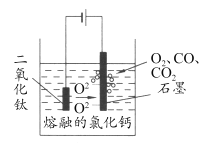
д�������缫��Ӧʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ����ͭ��Ũ���ᷴӦ��װ�á���ش�
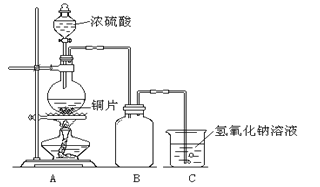
��1��д��ʢ����ͭƬ����������____________��
��2�����װ�������ԵIJ���Ϊ____________��
��3�������йظ�ʵ���˵������ȷ����____________��
A���ձ�������������Һ������������β������ֹ������Ⱦ
B��ʵ��ʱ���Թ۲쵽Բ����ƿ����Һ����ɫ���ձ�Ϊ��ɫ
C���� 0.08 mol ���ʵ�Ũ������������ͭƬ��Ӧ�����ռ���896mL����״������SO2
D���ڸ�ʵ����Ũ�������������Ժ�ǿ������
E����� B ��ʢ������ KMnO4 ��Һ����Ӧһ��ʱ����Թ۲쵽��ɫ��ȥ��˵��SO2����Ư���ԡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ�ͨ�����·ֽ�FeSO4�ķ����Ʊ�Fe2O3��Ϊ����FeSO4���·ֽ�IJ���������й�̽��ʵ�飬�ش��������⣺
ʵ��һ�����·ֽ�FeSO4��������ͼ��ʾ��ʵ��װ�ý���ʵ�顣
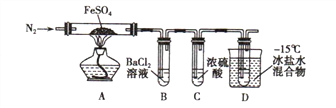
��֪����SO2�۵�Ϊ-72�棬�е�Ϊ-10�� �� SO3�۵�Ϊ-16.8�棬�е�Ϊ44.8��
��1������װ�ã��������������ã�����ҩƷ��ͨ��һ��ʱ��N2Ȼ����ȣ�ͨ��N2��Ŀ����_________________________
��2����������������650�棬����B���а�ɫ������D�Թ�������ɫҺ�壬Ӳ�ʲ������еĹ����Ϊ_________ɫ��д���÷�Ӧ�Ļ�ѧ����ʽ___________________��
��3����Ӧ��Ϻ�ֹͣ������ȴ��ȡӲ�ʲ������й��壬�����ᣬ��Ӧ�����ӷ���ʽ��__________________�� ����Ӧ��������Һ����D�Թ��У���Һ��Ϊdz��ɫ���÷�Ӧ�����ӷ���ʽ�� _______________
ʵ��� ̽�����·ֽ� FeSO4���ɵ�����
��4������ͼ��ʾװ�����ʵ�飬��֤���·ֽ�FeSO4���ɵ���̬����
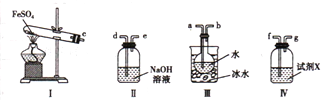
�ٰ������������Ӹ�����������ĸ��ʾ�ӿڵ�����˳��c-__________________________
���Լ�X�������� ___________________________
�۳�ַ�Ӧ������װ��III��Բ����ƿ�ڻ����ⶨ�ѷֽ��FeSO4 ����������Բ����ƿ�������Ȼ�����Һ��ֱ��������ȫ��Ȼ����˻����ڹ������Ͻ�����ϴ����ɲ���ȴ�����£����ء������յõ�����������ΪWg �����ѷֽ��FeSO4������ ________________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڴ�ˮ��25����80����pH( )
A��ǰ��С�ں��� B��ǰ�ߵ��ں��� C��ǰ�ߴ��ں��� D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�У�������ˮ�ĵ��룬ֻ�����±�����ʾ���������ӣ�.�����X�������༰�����bΪ
�������� | Na+ | Al3+ | Cl- | X |
���� | 2a | a | a | b |
A. NH4+��4a B. SO42-��2a C. OH-��4a D. CO32-��2a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ijЩ�������ȡ���ռ���β������װ����ͼ��ʾ(ʡ�Լгֺ;���װ��)�����ô�װ�úͱ����ṩ������������ʵ�飬�������ѡ����

ѡ�� | a�е����� | b�е����� | c���ռ������� | d�е����� |
A | Ũ��ˮ | CaO | NH3 | H2O |
B | Ũ���� | Na2SO3 | SO2 | NaOH��Һ |
C | ϡ���� | Cu | NO2 | H2O |
D | Ũ���� | MnO2 | Cl2 | NaOH��Һ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��е��������ƻ�1mol�����еĻ�ѧ�������ĵ�������kJ����
���� | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
������kJ�� | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
�����������ݻش��������⣺
��1���������ʱ������е�������͵��� ��
A��H2 B��Cl2C��Br2D��I2
��2��X2+H2![]() 2HX (X����Cl��Br��I)�ķ�Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ��
2HX (X����Cl��Br��I)�ķ�Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ��
��3����ͬ�����£�X2(X����Cl��Br��I)�ֱ���������Ӧ�������ĵ����ʵ���������ʱ���ų������յ����������� ��
��4�������ϱ��е����ݣ����ܻش����⣨3���� ���ش������������������������������ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com