
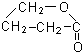 +2H2O.
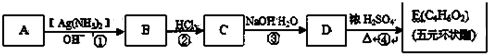
+2H2O. 分析 饱和一元醇X,通式CnH2n+2O,X中碳元素的质量分数约为65%,则12n÷(12n+2n+2+16)=65%,解得n=4,则X的分子式为C4H10O;A能与银氨溶液反应,含有醛基,1mol A和2mol H2在一定条件下恰好完全反应,除醛基外,还含有1个碳碳双键,A经过系列转化生成E为五元环酯,故A的结构简式为CH2=CHCH2CHO,CH2=CHCH2CHO与银氨溶液反应生成B,则B为CH2=CHCH2COOH,CH2=CHCH2COOH与氯化氢发生取代反应生成C,则C为ClCH2CH2CH2COOH,ClCH2CH2CH2COOH与氢氧化钠水溶液发生取代反应生成D,则D为HOCH2CH2CH2COOH,HOCH2CH2CH2COOH在浓硫酸作用下发生取代反应生成E,则E为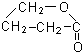 ,据此解答.
,据此解答.
解答 解:饱和一元醇X,通式CnH2n+2O,X中碳元素的质量分数约为65%,则12n÷(12n+2n+2+16)=65%,解得n=4,则X的分子式为C4H10O;A能与银氨溶液反应,含有醛基,1mol A和2mol H2在一定条件下恰好完全反应,除醛基外,还含有1个碳碳双键,A经过系列转化生成E为五元环酯,故A的结构简式为CH2=CHCH2CHO,CH2=CHCH2CHO与银氨溶液反应生成B,则B为CH2=CHCH2COOH,CH2=CHCH2COOH与氯化氢发生取代反应生成C,则C为ClCH2CH2CH2COOH,ClCH2CH2CH2COOH与氢氧化钠水溶液发生取代反应生成D,则D为HOCH2CH2CH2COOH,HOCH2CH2CH2COOH在浓硫酸作用下发生取代反应生成E,则E为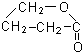 .
.
(1)由上述分析可知,X的分子式为:C4H10O,故答案为:C4H10O;
(2)A的结构简式为CH2=CHCH2CHO,含有的官能团有碳碳双键、醛基,故答案为:碳碳双键、醛基;
(3)D→E是HOCH2CH2CH2COOH在浓硫酸作用下发生取代反应生成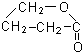 ,反应方程式为HOCH2CH2CH2COOH$→_{△}^{浓硫酸}$
,反应方程式为HOCH2CH2CH2COOH$→_{△}^{浓硫酸}$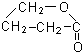 +2H2O,
+2H2O,
故答案为:HOCH2CH2CH2COOH$→_{△}^{浓硫酸}$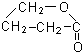 +2H2O.
+2H2O.
点评 本题考查有机物推断,计算确定A的分子式是关键,再结合转化关系及E的结构特点进行推断,需要学生熟练掌握官能团的性质与转化,能较好的考查考生的推理能力和知识迁移运用能力,是热点题型,难度中等.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案科目:高中化学 来源: 题型:解答题
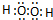 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 名称 | 结构简式 | 熔点/℃ | 沸点/℃ |
| 正丁烷 | CH3CH2CH2CH3 | -138.4 | -0.5 |
| 异丁烷 | CH(CH3)3 | -159.6 | -11.7 |
| A. | 正丁烷的所有碳原子在同一直线上 | |
| B. | 正丁烷、异丁烷常温下都为气态 | |
| C. | 气体打火机中所灌装的丁烷最有可能是正丁烷 | |
| D. | 相同碳原子数的烷烃,支链越多,沸点越低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | 向氨水中滴加氯化铝溶液:Al3++4OH-=AlO2-+2H2O | |
| C. | 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O | |
| D. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇(水):加入新制的生石灰,然后蒸馏 | |
| B. | 乙酸乙酯(乙酸):加入饱和碳酸钠溶液,然后分液 | |
| C. | 乙烷(乙烯):通入酸性高锰酸钾溶液中洗气 | |
| D. | 溴苯(溴):加入氢氧化钠溶液,然后分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com