
根据下图,下列判断中正确的是( )

A.烧杯a中的溶液pH降低
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-===H2↑
D.烧杯b中发生的反应为2Cl--2e-===Cl2↑
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
按要求回答下列问题
(1)相同温度、相同物质的量浓度的下列四种溶液,用序号按pH由大到小的顺序排列
①CH3COONa ②Na2CO3 ③NaCl ④苯酚钠 ⑤NaHCO3 ____________。
(2)某烃结构简式为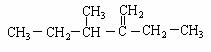 ,此烃名称为 。
,此烃名称为 。
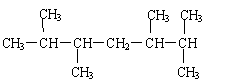 |
(3)某烷烃的结构简式为 ,其一氯代物有 种。
(4)用Na2CO3溶液除去苯中混有的苯酚,发生反应的离子方程式为 __ ,之后再进行 操作。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一支25 mL的酸式滴定管中盛入0.1 mol·L-1 HCl溶液,其液面恰好在5 mL的刻度处,若把滴定管中的溶液全部放入烧杯中,然后以0.1 mol·L-1 NaOH溶液进行中和,则所需NaOH溶液的体积( )
A.大于20 mL B.小于20 mL C.等于20 mL D.等于5 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应;⑤用惰性电极电解含B离子和E离子的溶液,E先析出。据此,判断五种金属的活动性顺序是( )
A.A>B>C>D>E B.A>C>D>B>E
C.C>A>B>D>E D.B>D>C>A>E
查看答案和解析>>
科目:高中化学 来源: 题型:
铝-空气海水电池:以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。
电池总反应为4Al+3O2+6H2O===4Al(OH)3
负极:________________________________________________________________________;
正极:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )
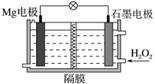
A.Mg电极是该电池的正极
B.H2O2在石墨电极上发生氧化反应
C.石墨电极附近溶液的pH增大
D.溶液中Cl-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
“ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
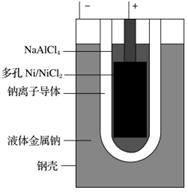
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三价铝离子
C.正极反应为NiCl2+2e-===Ni+2Cl-
D.钠离子通过钠离子导体在两电极间移动
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列有关叙述正确的是
A.标准状况下,44.8L苯中分子数为2NA
B.1mol水中含氢离子数为NA
C.5.6g铁与足量稀硫酸完全反应失去电子数为0.3NA
D.16 g CH4与18 g NH4+ 所含电子数均为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)硫、碳、硅是三种重要的非金属元素,请回答下列问题:
(1)它们的非金属性由强到弱的顺序是 (用元素符号表示),
| |
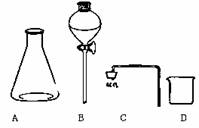
(2)请你用题中所给仪器设计一套装置证明(1)中的结论,在右边方框
中画出装置图;仪器B的名称是 。
(3)实验过程中在仪器B 中应装入的试剂是 ,烧杯中出现的现
象是 。若锥形瓶中装的是一种能溶于水的正盐,则
其中发生反应的离子方程式为 。
| |
(1)在右边方框中画出装置图。
(2)若实验时,M上有气泡,N上没气泡,则M的最高价氧化物对应
的水化物的碱性比N的最高价氧化物对应的水化物的碱性比
(填“强”或“弱”),外电路中电子由 (填M或N)极流
向 (填M或N)极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com