
 �����Ϊ1L�ĺ����ܱ������У�����1molCO2��3molH2��һ�������·�����ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g�������CO2��CH3OH��Ũ����ʱ��仯��ͼ��ʾ������˵����ȷ���ǣ�������
�����Ϊ1L�ĺ����ܱ������У�����1molCO2��3molH2��һ�������·�����ӦCO2��g��+3H2��g��?CH3OH��g��+H2O��g�������CO2��CH3OH��Ũ����ʱ��仯��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �û�ѧ��Ӧ��3minʱ�ﵽƽ��״̬ | |
| B�� | ���������������䣬�����¶ȣ�ƽ��ʱc��CH3OH��=0.85 mol•L-1����÷�Ӧ�ġ�H��0 | |
| C�� | ��ͬ�¶��£���ʼʱ�����������г���0.5molCO2��1.5molH2��ƽ��ʱCO2��ת����С��75% | |
| D�� | 12minʱ���������������ٳ���0.25molCO2��0.25molH2O��g������ʱ��Ӧ�����淴Ӧ������� |
���� A���ﵽƽ��״̬ʱ���淴Ӧ������ȣ���3minʱ�����Ũ����Ȼ�ڱ仯��
B��ƽ��ʱ�״���Ũ��Ϊ0.75mol/L������¶ȶԻ�ѧƽ���Ӱ���жϸ÷�Ӧ���ʱ䣻
C����ͬ�¶��£���ʼʱ�����������г���0.5molCO2��1.5molH2���൱�ڼ�С��ѹǿ������ѹǿ�Ը÷�Ӧ��Ӱ���жϣ�
D���ٳ���0.25molCO2��0.25molH2O��g������Ӧ��Ũ������ƽ�����������ƶ���
��� A������ͼ���֪���е�3����ʱ��CO2��CH3OH��g����Ũ����ͬ�����״��Ͷ�����̼��Ũ����Ȼ�����仯��˵����ʱû�дﵽƽ��״̬����A����
B������ͼ���֪10���Ӻ�CO2��CH3OH��g����Ũ�Ȳ��ٱ仯���ﵽ��ѧƽ��״̬��ƽ��ʱc��CH3OH��=0.75 mol•L-1�������¶Ⱥ�c��CH3OH��=0.85 mol•L-1��˵�������¶�ƽ�����������ƶ�����÷�ӦΪ���ȷ�Ӧ���÷�Ӧ�ġ�H��0����B��ȷ��
C��ԭ��Ӧ�ﵽƽ��ʱ������̼��ת����Ϊ��$\frac{1mol-0.25mol}{1mol}$��100%=75%����ͬ�¶��£���ʼʱ�����������г���0.5molCO2��1.5molH2����ԭƽ������൱�ڼ�С��ѹǿ��ƽ�����������ƶ��������´ﵽƽ��ʱCO2��ת����С��75%����C��ȷ��
D��12minʱ���������������ٳ���0.25molCO2��0.25molH2O��g������Ӧ��Ũ��������ƽ�����������ƶ�����D����
��ѡBC��
���� ���⿼�黯ѧƽ��ͼ��ѧƽ��ļ��㣬��Ŀ�Ѷ��еȣ�����ʱע��۲�ͼ�е�����������壬��ȷ��ѧƽ�⼰��Ӱ������Ϊ���ؼ�������������ѧ���ķ�����������������ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ��ͨ��������������SO2+2OH-�TSO32-+H2O | |
| B�� | ʯ��ˮ����ᷴӦ��CaCO3+2H+�TCa2++CO2��+H2O | |
| C�� | ����ˮ��Ӧ��Na+2H2O�T2OH-+Na++H2�� | |
| D�� | ������̼��������Һ�еμ���������ʯ��ˮ��HCO${\;}_{3}^{-}$+Ca2++OH-�TCaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Ƽӵ���ˮ�У�Na+2H2O�TNa++2OH-+H2�� | |
| B�� | NaHCO3��Һ�еμ�����Ca��OH��2��Һ��Ca2++OH-+HCO3-�TCaCO3��+H2O | |
| C�� | ��������Һ�м��������ˮ��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O | |
| D�� | ��2 mol/L AlCl3��Һ��7 mol/L NaOH��Һ�������ϣ�2Al3++7OH-�TAl��OH��3��+AlO2-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
��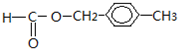 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol/L������Һ�У�c��H+��=c��CH3COO- ��+c��OH- �� | |
| B�� | �к�pH���������ͬ������ʹ��ᣬ����NaOH�������ߴ���ǰ�� | |
| C�� | ��ˮ�����H+Ũ��Ϊ1.0��10-4mol/L����Һ��pHһ������4 | |
| D�� | NaHCO3��Һ�У�c��Na+����c��HCO3-����c��H2CO3����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
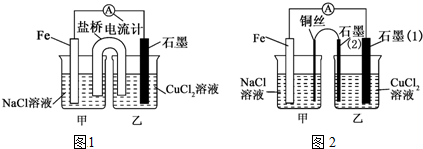
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ������Ũ�ȹ�ϵΪ��c ��Na+����c��HCO3-����c ��OH-����c��H+�� | |
| B�� | 25��ʱ����ˮϡ�ͺ�$\frac{c��O{H}^{-}��}{c��{H}^{+}��}$��С | |
| C�� | �¶����ߣ�c��OH-����c��H+�����䣨��������仯�� | |
| D�� | ��Һ��c��Na+��=c��HCO3-��+c��CO32-��+c��H2CO3�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com