
【题目】NA是阿伏加德罗常数的值。下列说法正确的是
A.22.4 L(标准状况)氮气中含有7NA个中子
B.1 mol重水比1 mol水多NA个质子
C.12 g石墨烯和12 g金刚石均含有NA个碳原子
D.1 L 1 mol·L1 NaCl溶液含有28NA个电子
科目:高中化学 来源: 题型:
【题目】下图装置中X和Y均为石墨电极,电解液为500mL某CuCl2溶液,电解时X电极表面有红色固体生成,Y电极有气体产生。一段时间后,取出X电极,洗涤、干燥、称量,电极增重1.6g。下列有关说法中正确的是
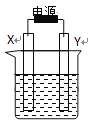
A. X电极连接电源正极
B. 生成气体体积为0.56L
C. Y电极上发生氧化反应
D. 该CuCl2溶液浓度为0.05mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
在反应①中,氧化剂是___,还原剂是___。在反应②中,氧化剂是__,还原剂是__。
(2)汽车尾气中含有二氧化氮和一氧化碳,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成氮气和二氧化碳,该反应的化学方程式为___。
(3)氨气亦可用来处理氮氧化物。例如,氨气与二氧化氮发生如下反应:6NO2+8NH3=7N2+12H2O。若某工厂排出的尾气中二氧化氮含量为0.5%(体积分数),处理1×103m3(标准状况)这种尾气,需要多少千克氨气___?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下图所示。下列说法中,错误的是
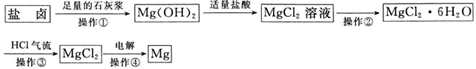
A.操作①发生的反应为非氧化还原反应
B.在实验室进行操作①时,只需要漏斗和烧杯两种玻璃仪器
C.操作②是蒸发浓缩、冷却结晶
D.在整个制备过程中未发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有下列物质①过氧化钠、②氧化铝、③硅、④二氧化硅、⑤NaHCO3。请填空:(填序号)
可用来制计算机芯片的是_________。可用于呼吸面具中作为氧气来源的是______。能作光导纤维的是_________。能作耐火材料的是_______。属于电解质的是 _________________。属于盐的是 ______,该盐受热分解的化学方程式为:_____________________________。
(2)除去FeCl2溶液中混有的FeCl3,相应的离子方程式是_______________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。
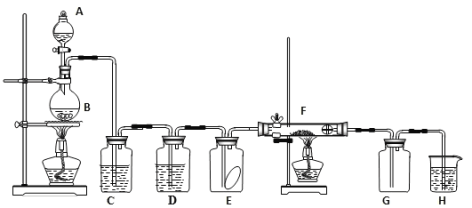
(1)装置C中盛装的溶液是____________,D中试剂的作用是____________________。
(2)E中的红色布条是否褪色?____(填“是”或“否”),写出F中反应的化学反应方程式:____________________,其反应现象为__________________________。
(3)H中的试剂为___________,用来吸收多余氯气。工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,该反应的化学方程式为_________________________。
(4)8.7gMnO2固体与足量浓盐酸充分反应,在标准状况下产生Cl2的体积为_____L;其中被氧化的HCl的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
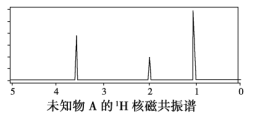
【题目】已知某有机物A的红外光谱和1H核磁共振谱如下图所示,下列说法中错误的是( )
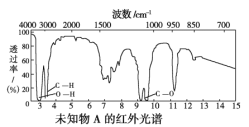
A. 由红外光谱图可知,该有机物中至少含有三种不同的化学键
B. 由1H核磁共振谱可知,该有机物分子中有三种不同的氢原子且个数比为1∶2∶3
C. 若A的化学式为C2H6O,则其结构简式为CH3CH2OH
D. 仅由其1H核磁共振谱就可得知其分子中的氢原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(FeSO4·7H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:烧渣![]()
![]() 溶液
溶液![]() 绿矾
绿矾![]() 铁黄。已知:FeS2和铁黄均难溶于水。下列说法不正确的是( )
铁黄。已知:FeS2和铁黄均难溶于水。下列说法不正确的是( )
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS2+14Fe3++8H2O═15Fe2++2SO42+16H+
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com